
Из какого кабинета в любой больнице периодически доносятся крики детей, а порой и взрослых? Что родители, нагло обманывая нас в детстве, сравнивали с укусом комарика? Я думаю вы уже догадались, что речь идет об анализе крови. Сейчас эта процедура стала более быстрой и менее болезненной. Не изменилось одно — ее важность. Диагностика в медицине играет самую важную роль на первых этапах борьбы с каким-либо заболеванием. Ведь чтобы победить недуг, его нужно сначала обнаружить. Пережив процедуру забора крови на анализ, вы спокойно отправляетесь ждать его результатов. В это время в лабораториях люди с помощью сложных, громоздких и весьма дорогих устройств анализируют вашу кровь, узнавая что в ней есть и в каком количестве. И хорошо, когда такая лаборатория есть в вашей местной больнице, но это не всегда так. А что если бы была карманная лаборатория, маленькая и недорогая, но при этом анализирующая образцы с той же точностью и эффективностью, что и обычная? Звучит, как научная фантастика, не так ли? Так же футуристично звучала и фраза «карманный анализатор сахара в крови» в свое время. Сегодня мы с вами познакомимся с исследованием и реализацией технологии количественного анализа белков и аминокислот посредством компактного устройства нового типа. Из чего состоит сие чудо, как оно работает и насколько эффективно? На эти и другие вопросы мы получим ответы в докладе ученых. Поехали.
Основа исследования
Мы живем в эпоху цифровых технологий, которые успешно внедряются в самых разных сферах нашей жизни. Лабораторные исследования (диагностические) не являются исключением. Ученые отмечают, что цифровой капельный анализ в 1000 раз точнее, чем традиционный, и позволяет проводить миллионы анализов параллельно в пределах одной капли образца объемом, измеряемым в фемтолитрах (фл, 1 фл = 10-15 л).
Использование цифрового анализа крайне полезно для обнаружения нуклеиновых кислот и белков, анализа отдельных клеток и даже экзосом.
Экзосомы* — внеклеточные пузырьки (диаметр: 30-100 нм), которые выделяются клетками в межклеточное пространство. Экзосомы участвуют в работе иммунитета, секреции белков и т.д.
На данный момент самыми известными цифровыми методами анализов являются dELISA (цифровой иммуноферментный анализ / цИФА) и цПЦР (цифровая полимеразная цепная реакция). Данные методики позволяют работать с отдельными клетками, получая при этом очень точные результаты, не требующие коррекции. Так недавно с помощью этих методов был осуществлен успешный количественный анализ белка и мРНК в одной клетке одновременно.
Подобные методики и демонстрация их талантов лишний раз показывают, что осуществление параллельного анализа в пределах крайне малой среды (образец) вполне возможно. Однако, как и любой другой технологии, у этих методов также есть недостатки. Они достаточно тривиальны — габариты, цена и сложность изготовления. Исследователи напоминают нам, что одна установка для цИФА (Quanterix’s Simoa) стоит порядка 100 000 долларов. А такую сумму может себе позволить далеко не каждая частная клиника, я уже молчу про государственные.
Конечно, этот «зверь» Quanterix’s Simoa очень мощный, если утрировать. В нем используются планшеты с микроячейками с 200 000 ячейками по 40 фл каждая.

Quanterix’s Simoa
При этом данное устройство может обрабатывать параллельно до 4 планшетов ELISA по 96 ячеек в каждом. Таким образом один аппарат способен в течение часа выдать результаты 66 образцов, каждый из которых может быть подвергнут 10-плексному анализу (т.е. 1 образец анализируется на 10 показателей одновременно). Цифры воистину невероятные. Но опять же возникает вопрос цены и габаритов такой чудо-машины.
Изображение №1
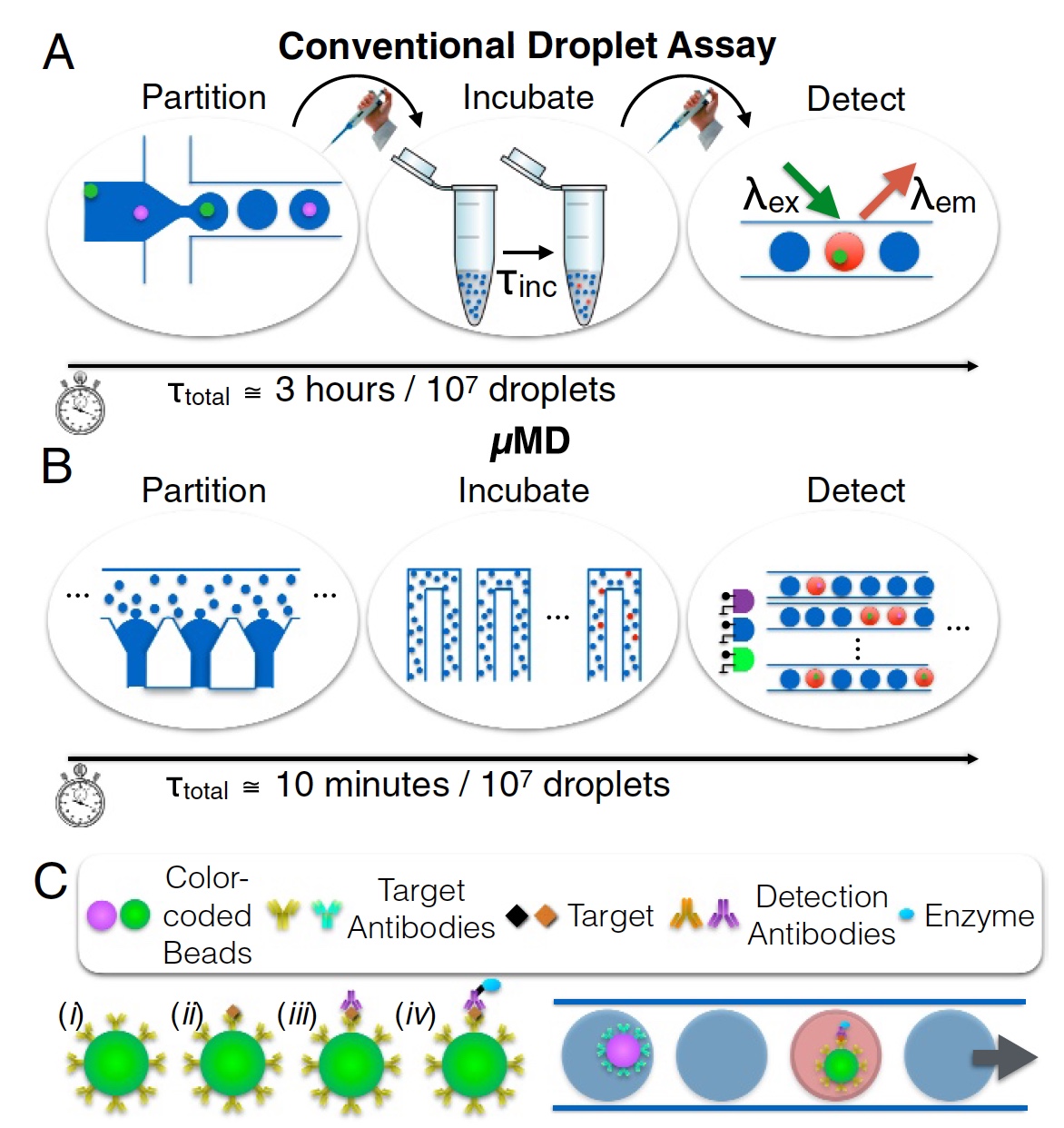
И тут ученые предлагают обратить свой взор в сторону микрофлюидных капельных систем. Классические системы такого рода не могут похвастаться колоссальными показателями Quanterix’s Simoa, однако могут послужить основой для нового устройства. Методика микрожидкостных капель с непрерывным потоком в теории может анализировать до 1 миллиона ячеек. Однако на практике такие показатели пока не были достигнуты ввиду нескольких причин. Во-первых, пропускная способность (менее 104 капель в секунду), когда капли генерируются последовательно (не параллельно) и являются монодисперсными. Во-вторых, обнаружение флуоресценции каждой капли проводится путем пропускания их по одной через лазерное пятно. Другими словами, все в очередь, по одному. Этот процесс показан на изображении 1а (разделение, инкубирование и определение; 3 часа на анализ 107 капель).
Основными же проблемами преобразования данного метода в компактный формат является сложность параллелизации оптики для мультицветного обнаружения флуоресценции, сложность интеграции процесса подготовки образцов и необходимость в определенных инструментах для генерации строго контролируемых потоков капель. Однако ученые не привыкли сдаваться перед лицом сложностей, какими бы внушительными они не были.
Микрокапельный Megascale Detector (MD, макро-детектор) это творение наших сегодняшних героев. Данное устройство не только может быть имплементировано в любое мобильное (карманное) устройство, но и соответствует стандартам количественного анализа обычных полноразмерных лабораторий. Процесс показан на изображении 1b (разделение, инкубирование и определение; 10 минут на анализ 107 капель).
Для достижения подобного, по словам исследователей, было реализовано три основные задачи:
- Вместо генерации по 1 капле, была использована параллельная генерация микрожидкосных капель, работающая в 100 раз быстрее. А наработки коллег-ученых в области производства монодисперсных капель (ссылка на данное исследование) позволили избавиться от зависимости монодисперсности капель от скорости потока. Это позволяет использовать очень недорогие перистальтические насосы, которые можно внедрить в мобильное (карманное) устройство.
- Быстрое считывание флуоресценции капель со скоростью более 105 в секунду (помните ограничение в 104, о котором я упоминал выше) было достигнуто благодаря визуализации на базе мобильного телефона, которая в 100 раз быстрее обычного считывания (когда капли считываются по очереди). В таком случае нет нужды в дорогостоящей оптике, а имплементация в карманные мобильные устройства очевидна. Основной отличительной чертой данного нововведения является возможность преодолеть ограничения низкой частоты кадров цифрового изображения и обеспечить многоцветное обнаружение флуоресценции путем модуляции нескольких источников возбуждения светодиодов или лазерных диодов разного цвета уникальными непериодическими сигналами. Видео можно декодировать для получения данных флюоресценции капли, преодолевая ограничения частоты кадров камеры. Таким образом можно достичь тех самых (о которых говорилось ранее) 1 миллиона капель в секунду.
- И наконец, интеграция блока обработки микрогранул (или микробусин, микроскопических сферических объектов), генератора капель, линий задержки сигналов для инкубации капель и детектора флуоресценции. Все вместе это дает недорогое, компактное и эффективное устройство для ввода необработанной сыворотки (образец) и вывода молекулярных данных (результат).
В качестве демонстрации своего изобретения ученые реализовали мультиплексированный цИФА с использованием микрогранул разного цвета, полученного за счет флуоресцентных красителей. Каждый цвет это цветовой «код» белка, на который нацелено антитело микрогранулы (1с).
Был проведен мультиплексный анализ цитокинов GM-CSF и IL6 в сыворотке с использованием ультрафиолетовых и зеленых флуоресцентных гранул, когда капли содержали микрогранулу с флуоресцентным красным иммунокомплексом. В качестве среды проведения количественного анализа была использована бычья сыворотка, а ограничение определения составило 0.004 пг/мл (пикограмм на миллилитр, 1 пг = 10−12 г). Это в 1000 раз точнее, чем у стандартного ИФА, и соответствует уровню точности цифрового ИФА.
На обработку 10 миллионов капель требуется всего лишь 10 минут. При этом сам процесс включает генерацию и инкубацию капель, а также обнаружение флуоресцентных капель для каждого образца.
Структура устройства и процесс анализа
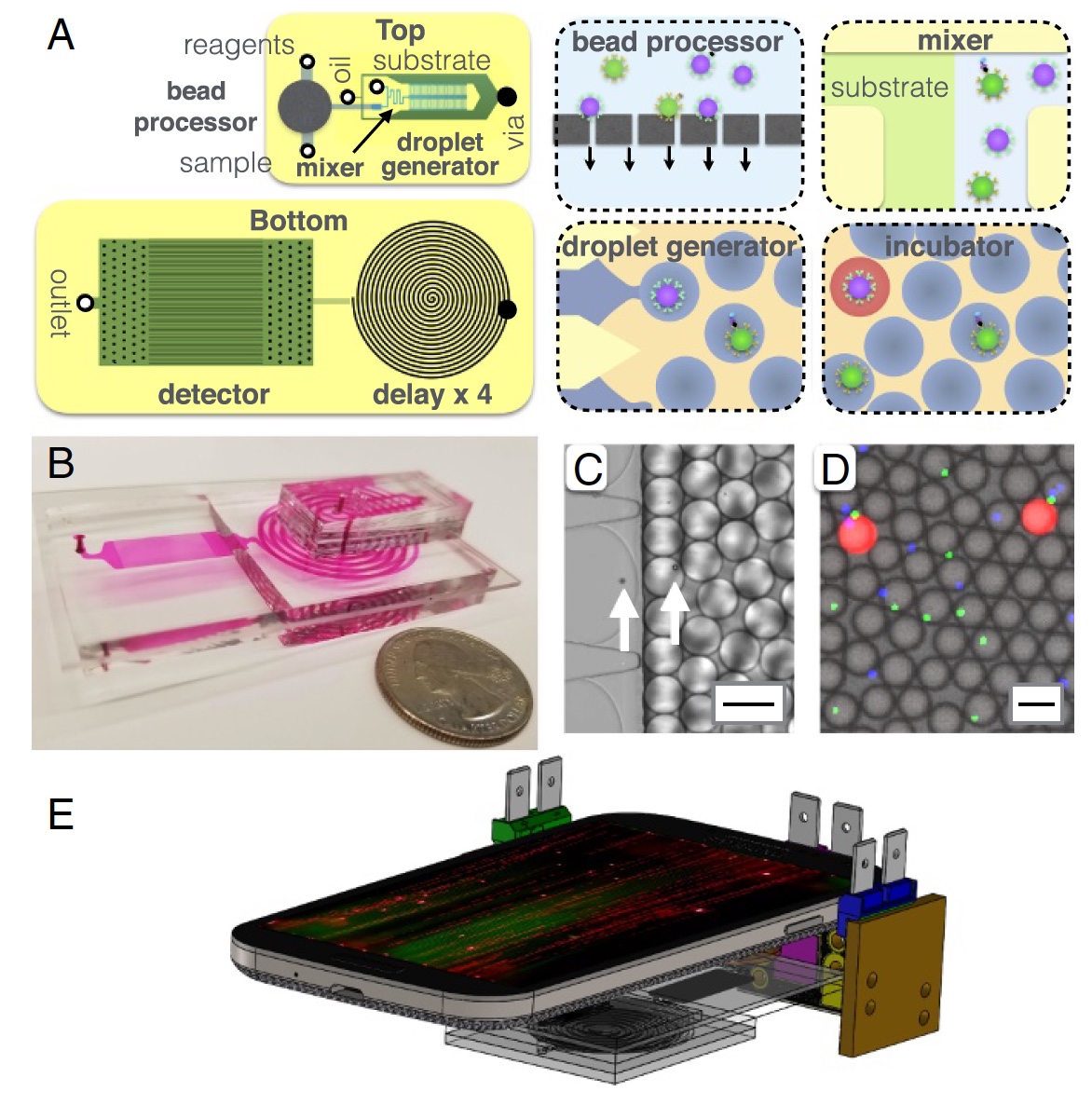
Изображение№2: структура MD устройства.
Немного подробнее об изображении выше: 2а — схема чипа, вид сверху и снизу; 2b — фото MD чипа, на котором видны все оптофлюидные каналы; 2с — микрофотография процесса инкапсулирования микрогранул в капли диаметром 40 мкм; 2d — флуоресцентная микрофотография капель после линии задержки; 2е — схематическое изображение MD платформы (мобильный телефон, 3 источника света и сам MD чип).
Основными составными частями MD можно назвать процессор микрогранул, где последние захватывают целевые белки из сыворотки. После этого гранулы помечаются иммунокомплексами для последующей амплификации внутри капель. Между каждым таким процессом происходит итеративная (несколько раз) очистка. Также присутствует генератор капель, где микрогранулы смешиваются с субстратом фермента и инкапсулируются в водно-масляные капли.
Следом идет микрожидкосный канал, по которому проходят в течение 3.2 минут капли. Этот канал необходим как задержка/замедление процесса, что позволяет ферментно усилить флуоресцентный сигнал. Заключительной частью является детектор (или сканер) на основе мобильного телефона (камеры), где и обнаруживается флуоресценция капель.
Процессор микрогранул состоит из полупроницаемой мембраны для иммобилизации гранул. К иммобилизованным гранулам доставляется несколько реагентов и промывочных буферов. После этого гранулы высвобождаются для дальнейшего анализа.
Сама мембрана сделана из поликарбоната. На мембране вытравлена дорожка площадью 300 мм2 с порами диаметром 3 мкм.
В данном эксперименте было две группы микрогранул: (d = 5,4 мкм, ex / em = 470/490 нм, CFH-5052-2), функционализированные антителом к GM-CSF (MAB2172) и (d = 4,5 мкм, ex / em = 370/410 нм, CFP-4041-2), функционализированные антителом к IL6 (MAB206).
Прежде всего микрогранулы проходят процесс инкубации вместе с образцом в течение 1 часа, и только после этого они захватываются на мембране, о которой упоминалось выше.
На данном этапе (в пределах мембраны) гранулы промывают 1 мл буфера T20 со скоростью потока 10 мл/ч, инкубируют с 0,1 мл 0,7 нМ детектирующего антитела в буфере T20 в течение 0.5 часа, еще раз промывают в 1 мл буфера T20 при 10 мл/ч, а уже после этого высвобождают из мембраны за счет изменения скорости потока до 6 мл/ч.
После этого освобожденные микрогранулы смешиваются с субстратом ИФА и инкапсулируются в капли диаметром 40 мкм. Для обеспечения точного смешивания гранул и субстрата и минимизации фонового сигнала от ферментов, генерирующих флуоресцентный сигнал, используется специальный канал длиной 14 мм.
Генератор капель сделан таким образом, чтобы диаметр капель не зависел от скорости потока. В данном устройстве всего 100 таких генераторов, которые на выходе дают пропускную способность в 100 000 капель в секунду.
Каждая капля инкапсулируется либо 1 гранулой, либо остается нетронутой. При этом достигается определенная концентрация — на 10 капель больше, чем микрогранул (например, 20 капель — 10 с гранулами и 10 без). Это уменьшает вероятность того, что в одной капле будет две гранулы до 0.5%.
Следом за генераторами капель идет линия задержки, похожая на спираль с шириной канала 1.8 мм и высотой — 1.5 мм. Линия задержки должна быть достаточно длинной, но при этом нельзя увеличивать устройство в размерах. Посему было сделано 4 спирали одна на одной, полностью пройти которые при скорости потока в 67 мл/ч каплям потребуется 3.2 минуты.
Для того, чтобы внедрить подобное устройство в мобильную платформу, необходимо было разрешить некие задачи, связанные с камерой телефона. Использование обычного постоянного по времени светового возбуждения приводит к тому, что движущиеся в поле зрение камеры капли визуализируются как полосы. Длина этой полосы устанавливает минимальное расстояние между каплями и, таким образом, серьезно ограничивает пропускную способность.
Если же использовать световое возбуждение с псевдослучайной последовательностью (по времени), это позволит «видеть» отдельные капли. Скорость модуляции света в 10 раз превышает время экспозиции камеры. За счет этой разницы капли формируют полосы, расстояние между которыми (три диаметра капли) достаточно для их индивидуального определения. При этом можно пропустить 120 параллельных капельных каналов перед камерой.
Другой важный момент в обнаружении и сканировании это флуоресценция. Для того, чтобы проводить мультиплексные ИФА, необходимо несколько разных флуоресцентных сигналов.Для этого было использовано сразу 3 источника света, каждый из которых обладает длиной волны, необходимой для возбуждения определенного флуоресцентного красителя. Данная тройная система состоит из двух диодных лазеров (синий, зеленый) и одного светодиода (УФ).
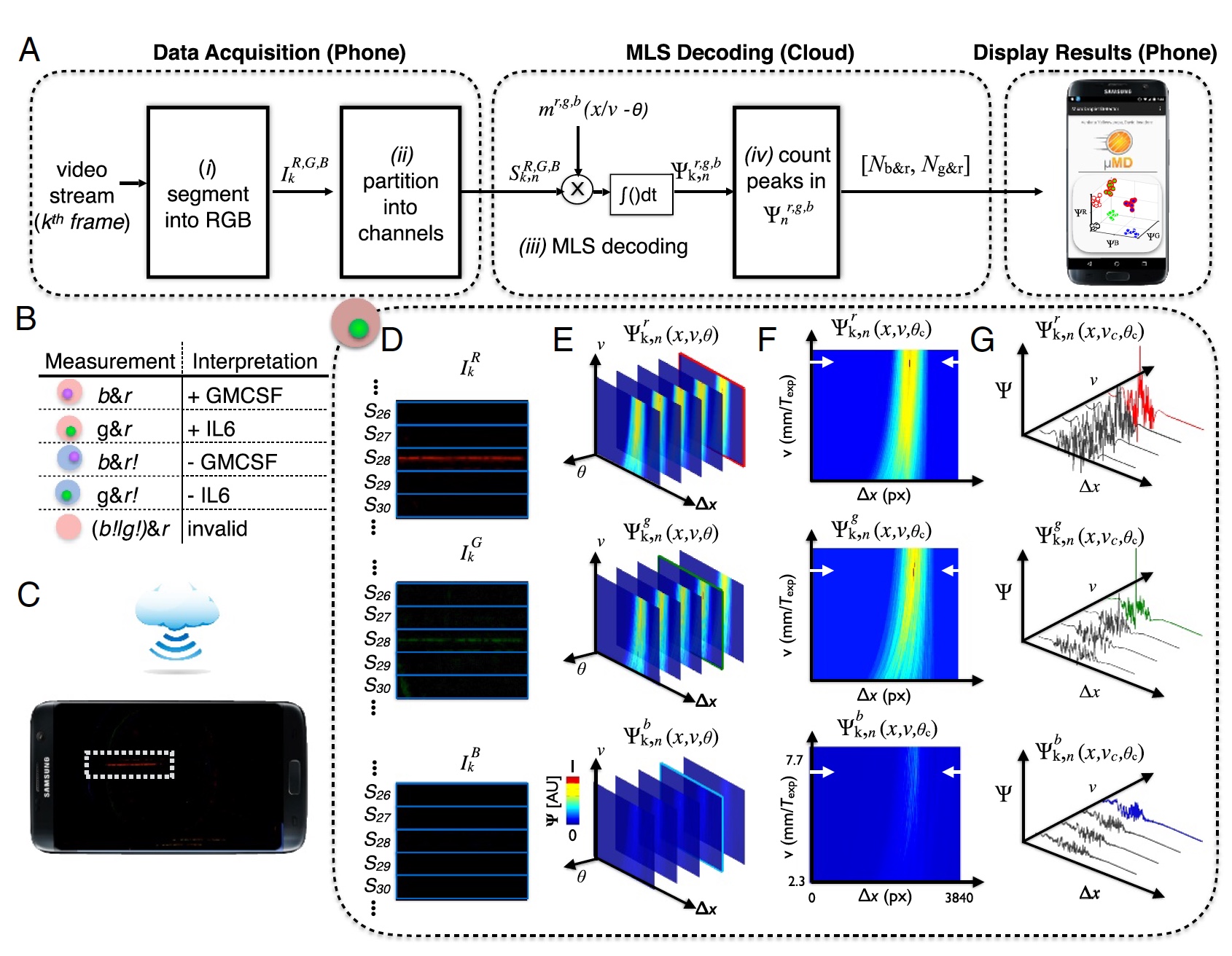
Изображение №3: процесс «образец-результат» (декодирование данных с камеры телефона).
Для точного декодирования видео с камеры телефона необходимо было провести обнаружение корреляции для трех ожидаемых паттернов модуляции (m), которые соответствуют каждому из трех источников света.
В результате получился вектор корреляции (3а), где: k — кадры; n=1:120 каналов в устройстве; R, G, B — цветовые каналы цифровой камеры; r, g, b — цветовое возбуждение.
Паттерн капель создавался посредством последовательности максимальной длины (MLS) с |m| = 63 бита. При этом каждый бит это 10 пикселей на цифровом изображении, то есть суммарно 63 бита это 630 пикселей (1/3 кадра шириной в 1920).
Флуоресцентное сканирование необходимо для того, чтобы определить содержит ли капля микрогранулу, если да — определить цвет (УФ или зеленый — белок, красный — целевая молекула). После получения этих данных, их необходимо извлечь. Для этого кадр видео разделяется на красный, зеленый и синий компоненты в соответствии с сенсорами камеры (3d).
В данном устройстве использовались облачные технологии. Это было сделано для снижения нагрузки на железо (то есть на сам телефон). Вместо контроля над скоростью капли или фазой, проводились облачные вычисления для определения капель с неизвестной фазой или скоростью (3с). После определения оптимальных фаз и скорости капли можно точно определить пики в корреляционном пространстве Ψr,g,bk,n(x, υc, θc) (3f и 3g).
Собранные данные загружаются в специальное приложение (пока только на ОС Android), которое отправляет их в облако для обработки с помощью MATLAB на удаленном сервере. После этого уже обработанные данные возвращаются на смартфон и отображаются на экране.
После проведения всех подготовительных и испытательных работ ученые решили провести «спарринг» с участием своего творения и уже существующего коммерческого полноразмерного устройства Simoa.
В испытательной дуэли использовались три варианта рабочей среды: PBS — натрий-фосфатный буфер, FBS — фетальная бычья сыворотка и сыворотка крови человека. Самым же важным показателем был предел обнаружения (LOD), то есть минимальное содержание определяемого вещества в образце.
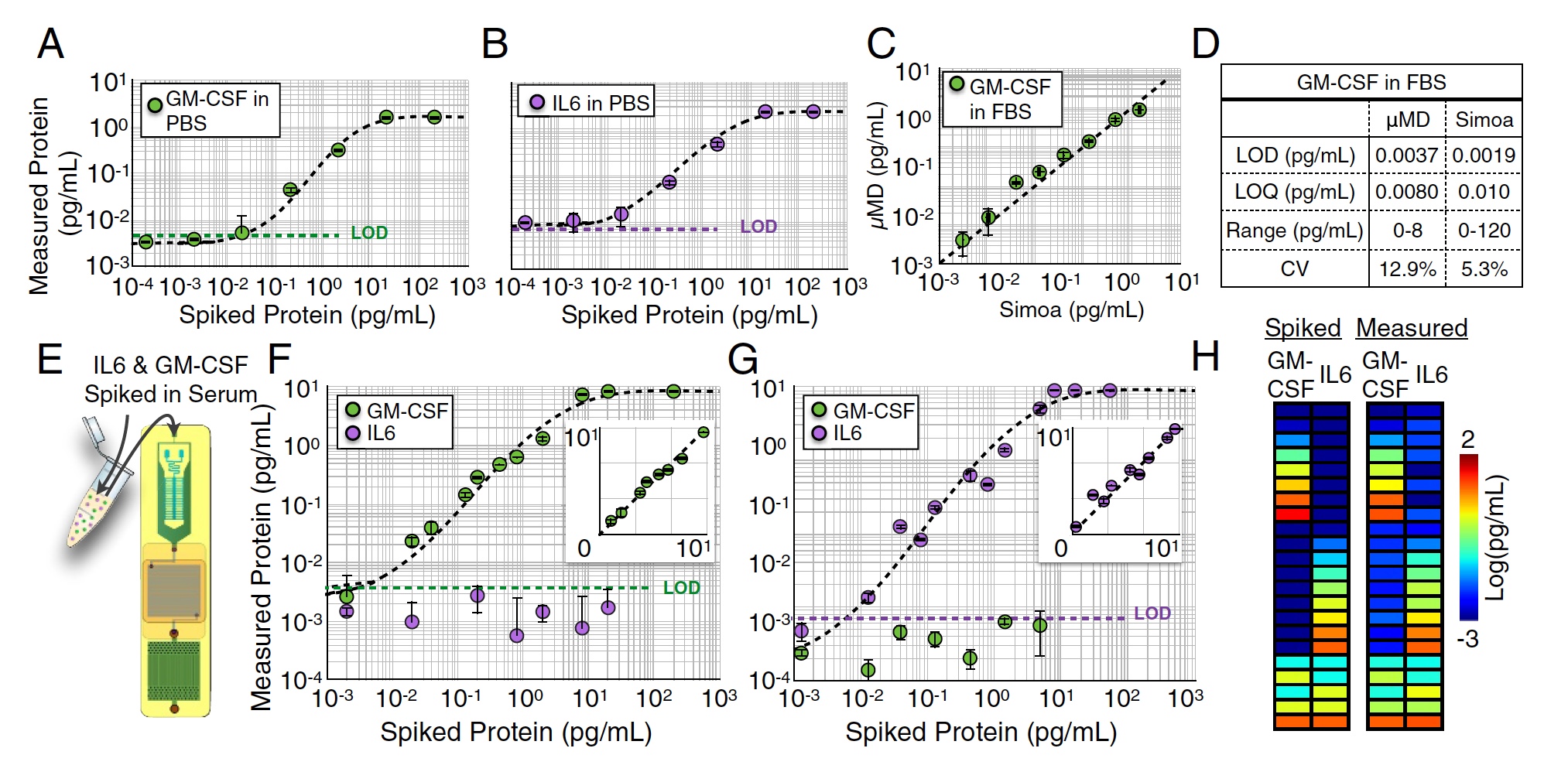
Результаты испытаний чипа MD.
В среде PBS было проведено несколько одноплексных измерений M-CSF (изображение А выше) и IL6 (изображение В) путем замера серийных разведений от 104 до 102 пг/мл. В этом тесте были получены очень хорошие показатели предела обнаружения: LOD = 0.0045 пг/мл для GM-CSF и LOD = 0.0070 пг/мл для IL6.
Подобные измерения также были проведены и в растворе FBS (1:4). На этом этапе образец для анализа был пополам разделен между исследуемым устройством и коммерческим «тяжеловесом» Simoa. В результате творение ученых показало отличные результаты, которые практически не уступали показателям Simoa (R2 = 0.95, изображение С выше).
Но это был одноплексный анализ, то есть анализ одного показателя. Теперь необходимо было проверить как чип MD будет справляться с параллельным анализом нескольких белков, то есть с дуплексным анализом GM-CSF и IL6 одновременно. Для начала в FBS было добавлено определенное количество GM-CSF, а концентрация IL6 была нулевой (изображения F и G). Потом было сделано наоборот: нулевая концентрация GM-CSF и какое-то количество IL6.
В обоих случаях показатели предела обнаружения не сильно отличались от результатов одноплексного анализа, проведенного ранее (p > 0.88 для GM-CSF и p > 0.90 для IL6).
После этого в образец было добавлено определенное количество и GM-CSF, и IL6 (изображение h). Точность обнаружения при этом была отличная — R2 > 0:99 для GM-CSF и R2 >0:99 для IL6.
Самым значимым тестом стал анализ сыворотки человека. Были взяты образцы крови у 14 испытуемых. Исследователи провели количественный анализ GM-CSF и IL6 этих образцов с помощью чипа MD и Simoa.

Результаты количественного анализа GM-CSF и IL6 человеческой сыворотки с помощью MD и Simoa.
Результаты анализа посредством чипа MD оказались очень близки к результатам Simoa (R2 =0:96), который на данный момент является самым точным анализатором.
Демонстрация устройства.
Для более детального ознакомления с нюансами и подробностями исследования рекомендую заглянуть в доклад исследовательской группы и дополнительные материалы к нему.
Эпилог
Скорость играет огромную роль в медицине. Чем быстрее будет проведена точная диагностика, тем быстрее можно начать лечение. Порой речь идет даже не о днях, а минутах, которые нельзя терять впустую. Однако время не всегда является основным фактором, когда у вас просто-напросто нет инструментов для проведения диагностики. Габариты, сложность производства и цена некоторых точных устройств для анализа, а также оборудование лабораторий всем необходимым доступно далеко не везде и далеко не всем.
Создание устройств, подобных чипу MD, это не просто хорошая затея, это гениальная и невероятно важная затея. Недорогой анализатор, который при этом демонстрирует отличную точность и скорость работы может сильно повлиять на медицину во всем мире, в частности в тех регионах, где использование стандартных средств невозможно. По словам самих ученых стоимость прототипа такого устройства составляет порядка 500 долларов. При массовом производстве цена для потребителя составит всего-навсего 5.
Право на лечение имеют все, однако по множеству причин это право далеко не всегда и не везде сопоставимо с реальностью. Подобные исследования и подобные устройства помогут изменить это.
Благодарю за внимание, оставайтесь любопытствующими и хорошей всем рабочей недели, ребята.
Спасибо, что остаётесь с нами. Вам нравятся наши статьи? Хотите видеть больше интересных материалов? Поддержите нас оформив заказ или порекомендовав знакомым, 30% скидка для пользователей Хабра на уникальный аналог entry-level серверов, который был придуман нами для Вас: Вся правда о VPS (KVM) E5-2650 v4 (6 Cores) 10GB DDR4 240GB SSD 1Gbps от $20 или как правильно делить сервер? (доступны варианты с RAID1 и RAID10, до 24 ядер и до 40GB DDR4).
VPS (KVM) E5-2650 v4 (6 Cores) 10GB DDR4 240GB SSD 1Gbps до лета бесплатно при оплате на срок от полугода, заказать можно тут.
Dell R730xd в 2 раза дешевле? Только у нас 2 х Intel Dodeca-Core Xeon E5-2650v4 128GB DDR4 6x480GB SSD 1Gbps 100 ТВ от $249 в Нидерландах и США! Читайте о том Как построить инфраструктуру корп. класса c применением серверов Dell R730xd Е5-2650 v4 стоимостью 9000 евро за копейки?
Источник

