
Вы когда-нибудь пытались объяснить трехлетнему ребенку, что такое атомы? Нет? И правильно, ибо впоследствии ребенок будет бегать по всему дому, детской площадке и магазину, тыкать пальцем на любой предмет и спрашивать «И тут тозе атомы?». Если же серьезно, любопытство, присущее детям, это то, что часто становится движущей силой многих открытий взрослых дядь и теть в белых халатах. Возвращаясь к атомам, все мы знаем, что они являются основными строительными кирпичиками всего, что нас окружает, и нас в том числе. Цементом, связывающим атомы между собой, являются заряженные частицы (ядра или электроны). Разные вещества формируются за счет разных вариантов взаимодействия (связи) электронов. Ученые из Нагойского университета (Япония) обнаружили, что охлажденный до -58 °C оксид вольфрама цезия (CsW2O6) демонстрирует необычную связь электронов, которую ранее обнаруживали исключительно в триводородных ионах, найти которые можно в межзвездном пространстве. Как подобная связь электронов влияет на свойства материала, в чем ее уникальность и что это значит для будущих исследований в области материаловедения? Ответы на эти вопросы мы найдем в докладе ученых. Поехали.
Основа исследования
Авторы сего труда отмечают, что понимание фазовых переходов кристаллических твердых тел является одной из основных задач в материаловедении. Сюда относится и электронные фазовые переходы в соединениях переходных металлов с пирохлорными* структурами, состоящими из трехмерных сетей тетраэдров.
Пирохлор* — минерал из класса оксидов и гидрооксидов, являющийся сложным оксидом натрия, кальция и ниобия с дополнительными анионами. Формула пирохлора выглядит так: (NaCa)2Nb2O6 (OH,F).
В качестве примера ученые приводят магнетит Fe3O4, который демонстрирует переход металл-диэлектрик*, сопровождаемый зарядовым упорядочением Fe при 119 К, называемым переходом Вервея*.
Переход металл-диэлектрик* обозначает, что вещество при определенных условиях демонстрирует свойства металла (например, проводимость), а при других условиях свойства изолятора.
Переход Вервея* — фазовый электронно-упорядочеваемый переход, который происходит в смешанновалентной системе и приводит к упорядочению формальных валентных состояний в низкотемпературной фазе.
Полного понимания этого перехода пока нет, хоть и было проведено множество исследований и опытов. Тем не менее, научное сообщество уделяет все больше внимания изучению переходов металл-диэлектрик, сопровождаемых магнитным упорядочением «все в одном» в 5d-оксидах (например, Cd2Os2O7 и Nd2Ir2O7). Основной причиной популярности таких переходов является возникновение ферроического упорядочения протяженных магнитных октаполюсов и образование фермионов Вейля* в твердом теле.
Фермион Вейля* — безмассовый тип фермиона со спином 1/2.
Фермион* — частица с полуцелым значением спина. К фермионам относятся кварки (протоны и нейтроны), лептоны (электроны, мюоны, тау-лептоны, нейтрино), дырки (квазичастицы в полупроводнике), а также квантовомеханические системы, состоящие из нечетного числа фермионов.
В данном исследовании ученые описывают самоорганизацию 5d электронов при электронном фазовом переходе β-пирохлора оксида CsW2O6, обнаруженную в высококачественных монокристаллах. Ранее сообщалось, что CsW2O6 обладает кубической решеткой с пространственной группой Fd3m при комнатной температуре. В таком случае атомы W образуют структуру пирохлора и имеют валентность 5.5+ с электронной конфигурацией 5d0.5. Измерение удельного электрического сопротивления поликристаллических образцов показало, что переход металл-диэлектрик происходит при температуре 210 К (-63.15 °C).
Также ранее сообщалось, что кристаллическая структура диэлектрической фазы имеет орторомбическую пространственную группу Pnma. Однако теоретические исследования показали, что это не соответствует действительности. Расчеты электронной структуры Fd3m фазы показали, что существует сильное влияние поверхностей Ферми, которое вызывает понижение симметрии до пространственной группы P4132.
* Pnma, Fd3m и другие относятся к кристаллографическим группам симметрии, которые описывают все возможные симметрии бесконечного количества периодически расположенных в трехмерном пространстве точек. Более детальную информацию касательно кристаллографических групп можно найти тут.
Недавние фотоэмиссионные эксперименты с тонкими пленками образцов показали, что валентность W в диэлектрической фазе диспропорционирует в 5+ и 6+.
Результаты исследования
Для начала стоит рассмотреть фазовый переход, который происходил при температуре 215 К.
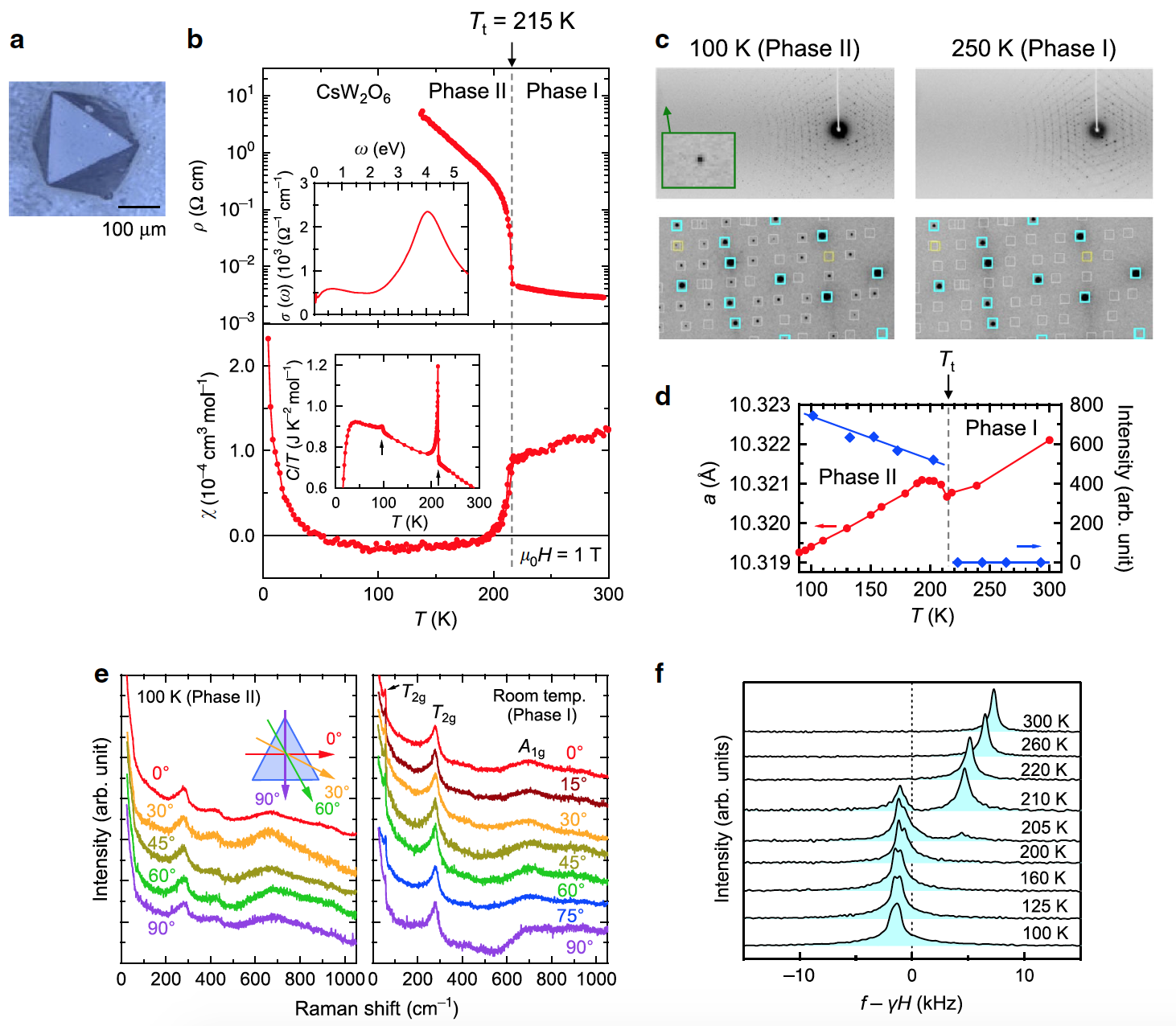
Изображение №1
В кварцевой трубке были подготовлены монокристаллы CsW2O6 (1а) и W-дефицитного CsW1.835O6. На графике 1b видно, что удельное сопротивление (p) монокристалла CsW2O6 сильно возрастает при понижении температуры ниже отметки Tt = 215 К, что наблюдалось и в случае поликристаллических образцов и тонких пленок.
Это увеличение сопротивления сопровождается небольшим, но вполне очевидным гистерезисом температуры. Это указывает на то, что фазовый переход первого рода происходит именно при Tt (т.е. при 215 К). В данном исследовании фазы выше и ниже Tt называются фаза I и фаза II соответственно.
Магнитная восприимчивость (χ) сильно уменьшается ниже Tt (1b), что также идентично поликристаллическому образцу. Однако линейная ширина спектров 133Cs-ЯМР в фазе II не показывает какого-либо значительного уширения по сравнению с фазой I (1f). Из этого следует, что уменьшение χ в фазе II не вызвано антиферромагнитным упорядочением.
На изображении 1с показаны рентгенограммы монокристалла CsW2O6, полученные при 250 К (фаза I) и 100 К (фаза II). Каждое из дифракционных пятен при 250 K было проиндексировано на основе кубической ячейки a = 10.321023(7) Å с пространственной группой Fd3m, в соответствии с предыдущими исследованиями. На дифракционной картине при 100 К появляется больше дифракционных пятен. Все они были проиндексированы на основе кубической пространственной группы P213 с постоянной решетки a = 10.319398(6) Å, что практически идентично a фазы I. Подобное изменение дифракционных пятен происходит при Tt, как видно из температурной зависимости интенсивности (1d).
Также стоит отметить, что в фазе II дифракционные пятна не разделяются на несколько пятен и не меняют свою форму даже в области высокого угла (1с). Класс Лауэ* и кристаллическая система, определяемые наблюдаемыми отражениями, ясно указывают на то, что структурное изменение, которое сохраняет кубическую симметрию, происходит при Tt, а фаза II имеет класс Лауэ m3.
Классы Лауэ* — кристаллографический класс симметрии, у которого есть центр симметрии. Из всех 32 классов лишь 11 считаются классами Лауэ. Класс m3 это дитригонально-пирамидальная система.
Как видно из поляризационной зависимости Рамановских спектров поверхности (111), измеренных при 100 К (фаза II) и комнатной температуре (фаза I на 1e) спектры фазы II не зависят от угла поляризации, как в фазе I. Это свидетельствует о наличии трехкратной вращательной симметрии, перпендикулярной (111), что согласуется с предполагаемой кубической симметрией.
Данные результаты означают, что структурная модель Pnma, предложенная на основе данных порошковой дифракции*, является неверной.
Порошковая рентгеновская дифракция* — метод исследования вещества путем дифракции рентгеновских лучей на образце в виде порошка.
Дополнительным подтверждением ошибочности Pnma является факт того, что данная модель имеет псевдотетрагональное искажение около 0.03%, но в данном исследовании этого не наблюдалось.
В поликристаллическом образце CsW2O6 W-дефицитный CsW1.835O6 всегда существует в качестве примесной фазы. Ученые считают, что в процессе определения природы фазы II важную роль сыграл факт того, что монокристаллы CsW2O6 и W-дефицитного CsW1.835O6 были получены отдельно, а измерения дифракционных и физических свойств выполнялись именно на монокристаллах.
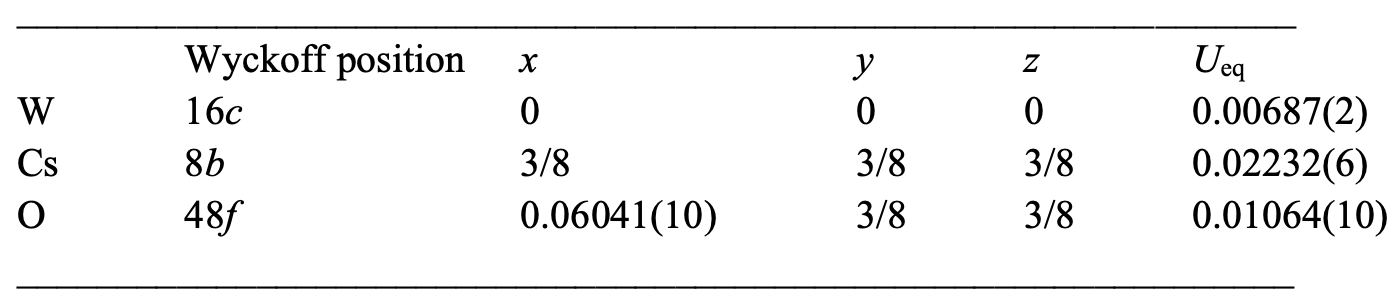
Таблица №1: кристаллографические данные CsW2O6 фазы I (250 К).
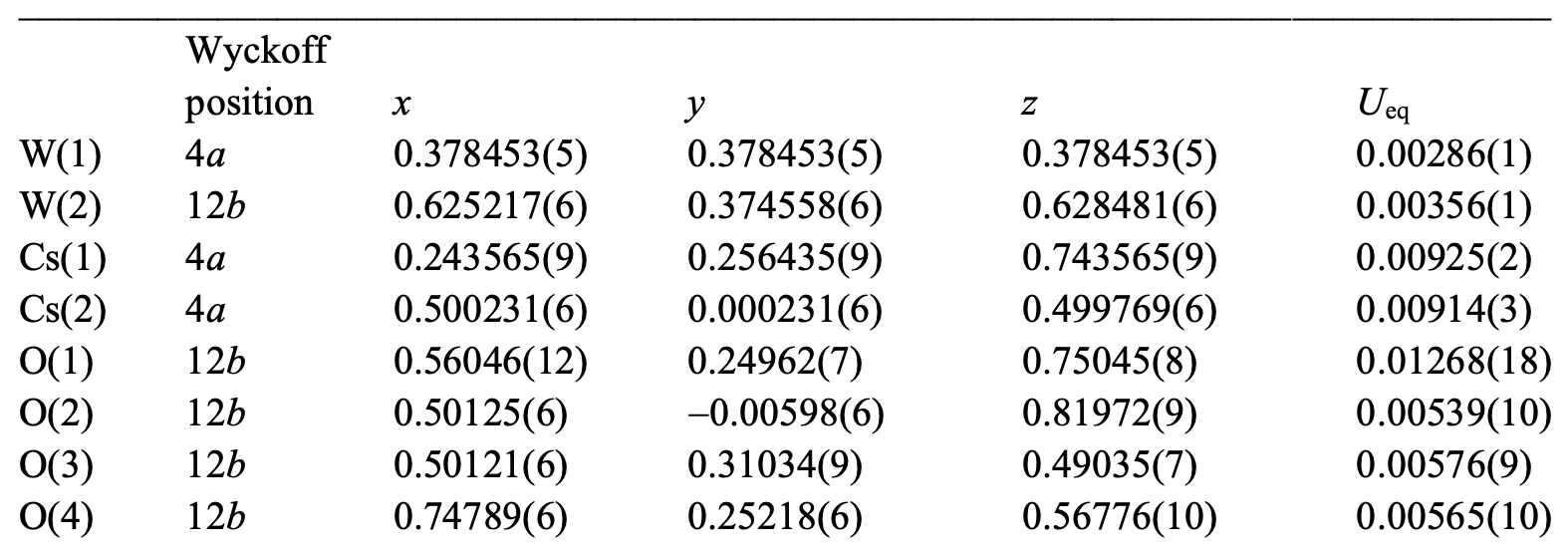
Таблица №2: кристаллографические данные CsW2O6 фазы II (100 К).
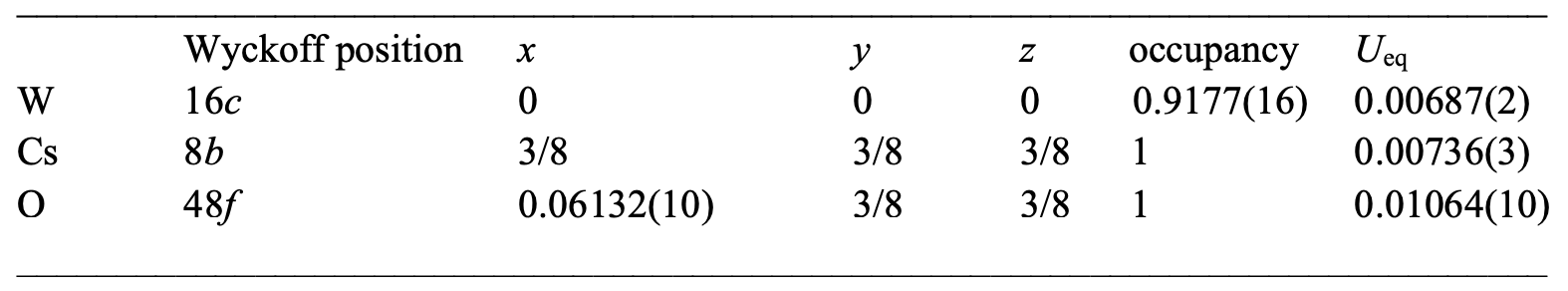
Таблица №3: кристаллографические данные CsW1.835O6 (30 К).
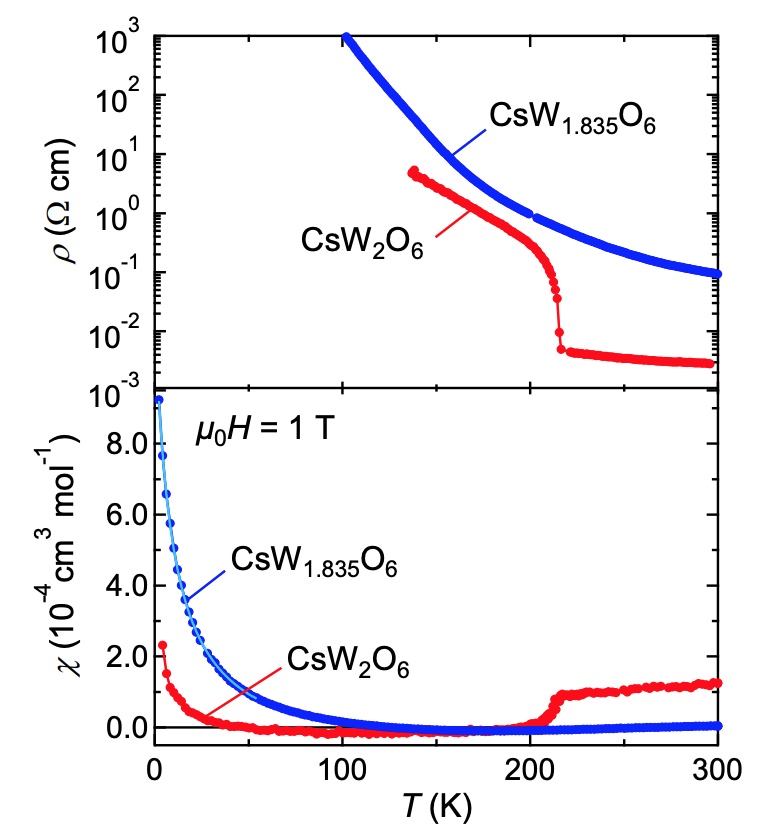
Температурная зависимость сопротивления (вверху) и магнитной восприимчивости (внизу) монокристаллов CsW1.835O6.
На следующем этапе исследования ученые более детально рассмотрели кристаллическую структуру фазы II.
В фазе I с пространственной группой Fd3m каждый из атомов Cs, W и O занимает один участок, где атомы Cs и W образуют структуры алмаза и пирохлора соответственно (2а).
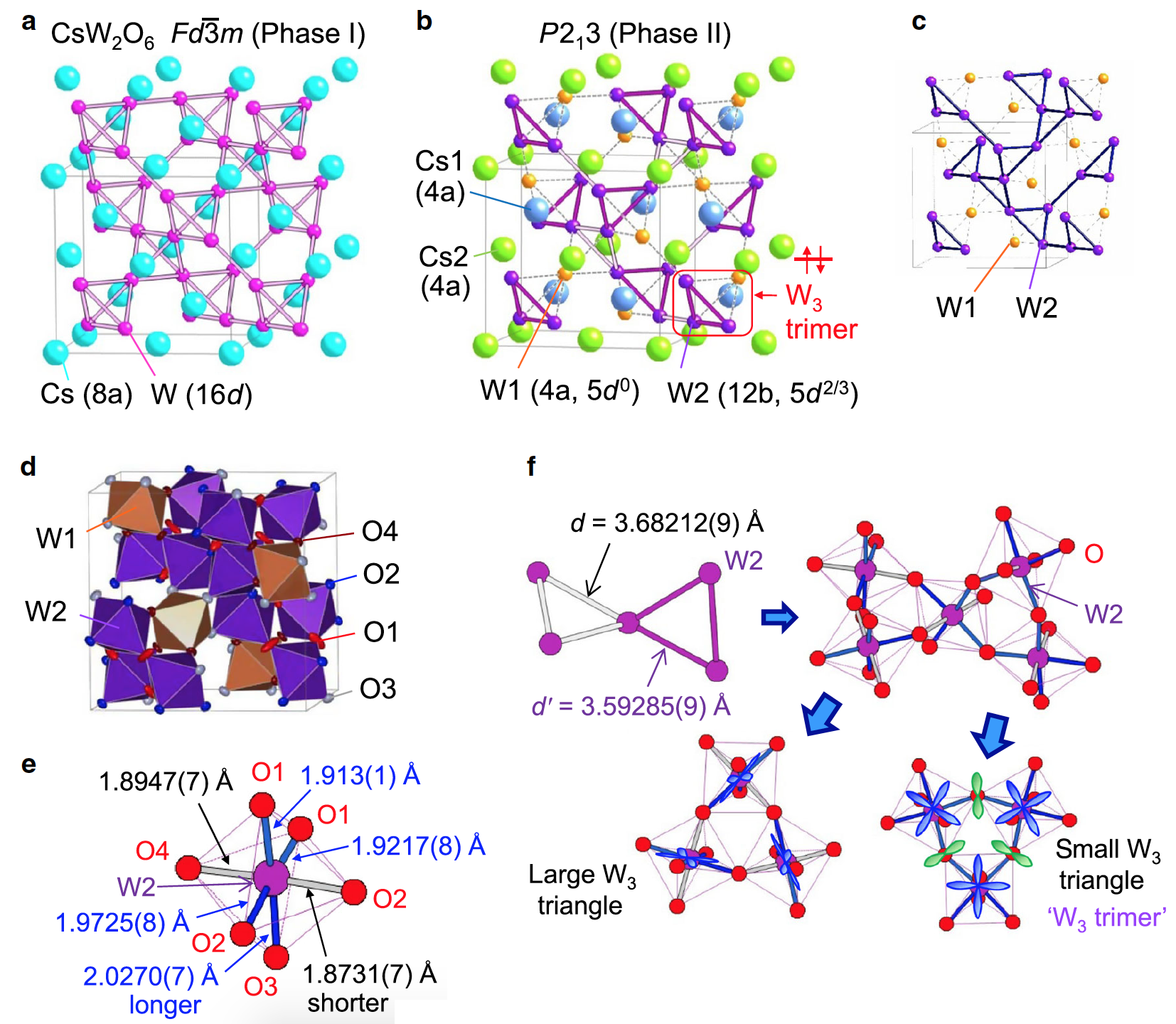
Изображение №2
В фазе II с пространственной группой P213 атомы Cs занимают два разных центра и образуют структуру «сфалерит» (названную в честь одноименного минерала, также именуемого «цинковая обманка*») (2b).
Обманками* называют минералы, которые не являются металлическими рудами, но обладают полуметаллическим блеском и другими признаками (цвет, плотность), присущими как рудам металлов, так и минералам.
Это было дополнительно подтверждено двумя пиками в спектрах 133Cs-ЯМР, соответствующими двум областям Cs, которые проявляются в виде небольшого расщепления пиков в случаях 200, 160 и 125 K (1f).
С другой стороны, атомы W занимают два участка с соотношением 1:3 в фазе II (2b и 2c), что несовместимо с зарядовым упорядочением W5+ – W6+ атомов W5+ и W6+ в соотношении 1:1.
В соответствии с расчетом валентной суммы связи для расстояний W – O, определенным из рентгеноструктурного анализа монокристалла, валентности атомов W(1) и W(2) была равна 6.07(3) и 5.79(3) при 100 К (фаза II) соответственно.
Учитывая, что параметры валентной суммы надежной связи W6+ доступны, а параметры W5+ — нет, логично, что атомы W(1) являются W6+ без 5d электронов. В этом случае валентность атомов W(2) становится равной 5.33+ с электронными конфигурациями 5d2/3.
Из вышеописанных расчетов следует, что зарядовое упорядочение с нецелой валентностью имеет место при Tt. Фактически, монокристаллы W-дефицитного CsW1.835O6, где все атомы W имеют валентность 6+ без 5d электронов, не показывают переход при Tt.
В фазе II атомы W(2) образуют трехмерную сеть из маленьких и больших правильных треугольников, которые поочередно связаны друг с другом общими углами (2b). Хотя разница в размерах между большим и малым треугольниками составляет около 2%, расположение занятых 5d-орбиталей между ними совершенно различно, что приводит к образованию тримера W3 в небольшом треугольнике. Если бы не было чередования треугольников W3, подрешетка W имела бы гиперкагомную (трехмерная структура из связанных треугольников) структуру (2с). Наличие чередования указывает на то, что структура «дышащего гиперкагома» (т.е. с зазорами, в отличие от равномерного гиперкагома) формируется во время фазы II.
Зарядовое упорядочение в фазе II CsW2O6 любопытно тем, что «условие Андерсона» поддерживается необычным образом. Андерсон говорил, что у магнетита есть бесконечное число моделей упорядочения зарядов, когда все тетраэдры в структуре пирохлора имеют одинаковый полный заряд (это и есть условие Андерсона), и это макроскопическое вырождение сильно подавляет температуру перехода Вервея.
Тем не менее, есть сведения о том, что не только магнетит, но и другие смешанно-валентные пирохлорные системы, такие как CuIr2S4 и AlV2O4, демонстрируют упорядочение зарядов, которое нарушает условие Андерсона. В таком случае энергия, полученная за счет σ-связи между d-орбиталями соседних атомов, должна быть достаточно большой, чтобы компенсировать потерю кулоновской энергии из-за нарушения условия Андерсона.
Но в случае с CsW2O6 ситуация иная. Его зарядовое упорядочение удовлетворяет условие Андерсона, где каждый тетраэдр состоит из трех атомов W5.33+ и одного атома W6+. Однако этот формат упорядочений отличается от предложенного Андерсоном и Вервеем, где валентности были целочисленные с соотношением 1:1.
Упорядочение гиперкагомного типа часто появляются в пирохлорных системах с соотношением двух видов атомов 1:3. Таким образом, CsW2O6 является на данный момент единственным примером упорядочения гиперкагомного типа с нетривиальной природой формирования.
Возникает вполне ожидаемый вопрос — почему именно такой формат упорядочения возникает в CsW2O6? По словам ученых, ответ можно получить, внимательнее рассмотрев неустойчивость поверхности Ферми электронной зонной структуры фазы I, т.е. понять движение и взаимодействие электронов в этой фазе.
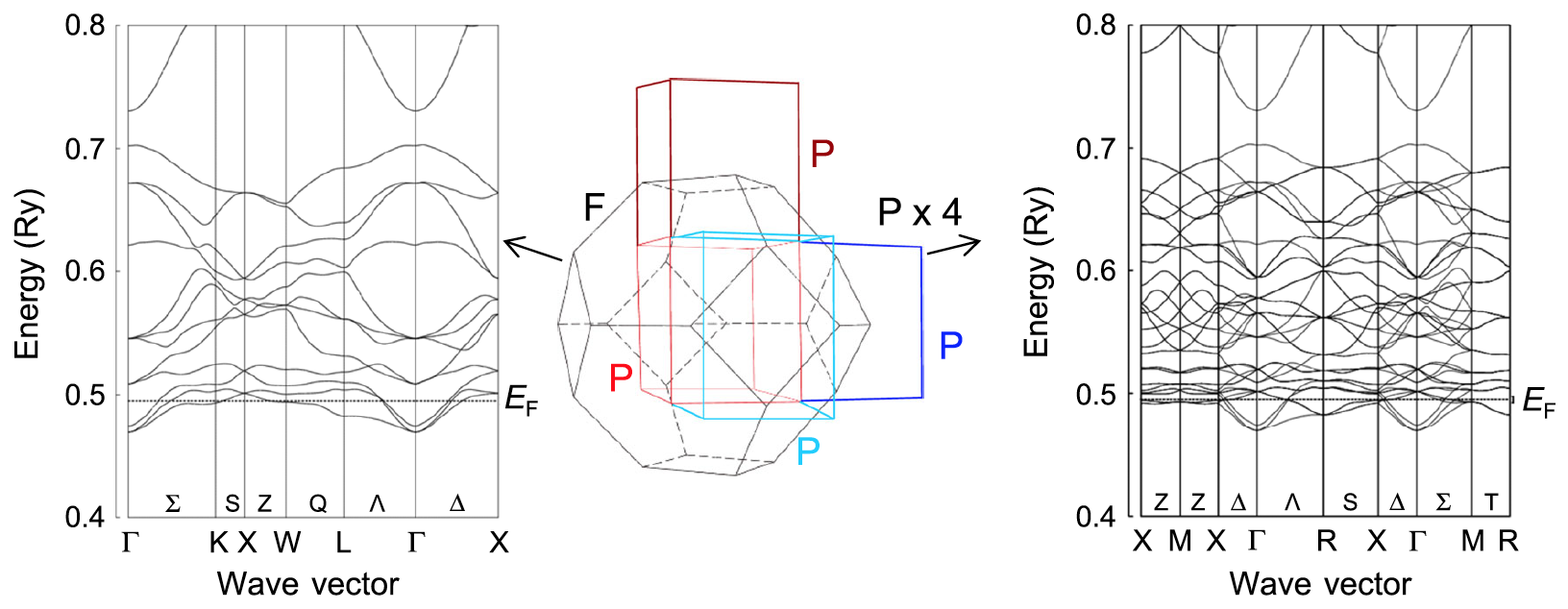
Изображение №3
Слева на изображении выше показана зонная структура фазы I, а справа — перекрывающие друг друга зонные структуры, полученные после параллельного сдвига электронных зон, соответствующих изменению примитивной ячейки с гранецентрированной сингонии на простую сингонию.
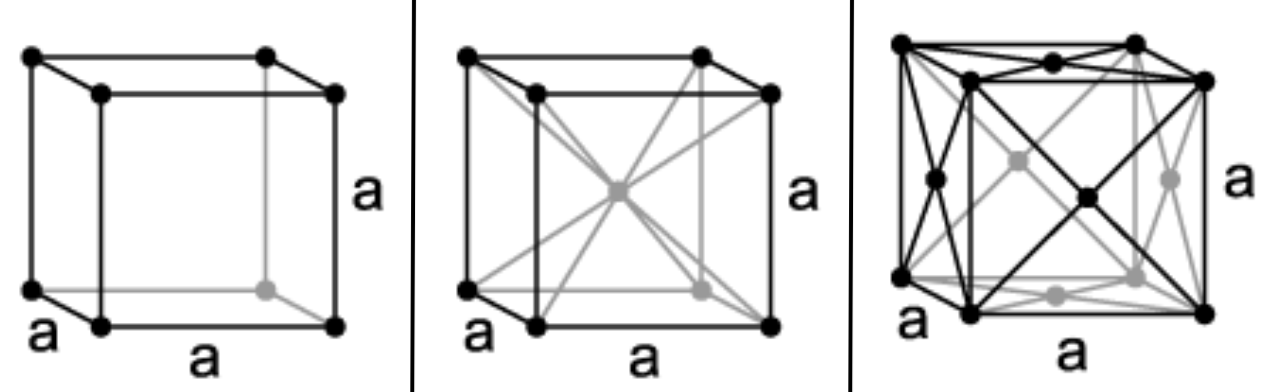
Кубическая сингония (слева направо): простая, объемно-центрированная и гранецентрированная.
Как видно на правой части изображения №3, пересечение зон происходит вблизи всех точек, где электронные зоны касаются энергии Ферми (EF). Следовательно, поверхности Ферми хорошо вложены за счет параллельных сдвигов электронных зон, соответствующих потере операций центрирования.
Подобный сценарий развития событий ученые именуют «трехмерной вложенностью». Это означает, что большая электронная энергия генерируется за счет структурных изменений, связанных с вышеупомянутым изменением симметрии. Следовательно, эта трехмерная вложенность может быть важным компонентом возникновения перехода при 215 К.
Если рассматривать данный эффект как единственную движущую силу в возникновении перехода, то должно произойти структурное изменение с Fd3m на P4132 или P4332, что уже высказывалось в ранее проведенном теоретическом исследовании. В таком случае атомы W(2) должны образовывать однородную гиперкагомную структуру. Также предполагается, что запрещенная зона не открывается при энергии Ферми в случаях P4132 и P4332, что не согласуется с наблюдаемой в данном исследовании диэлектрической природой фазы II.
В действительности же пространственной группой фазы II является P213, которая является подгруппой P4132 и P4332, а атомы W(2) образуют дышащую гиперкагомную структуру, где размер маленького треугольника на 2% меньше, чем у большого.
Кроме того, ориентация занятых 5d орбиталей важна для понижения симметрии с P4132 / P4332 (равномерный гиперкагом) до P213 (дышащий гиперкагом). Для октаэдра W(2)O6 фазы II (2е) две апикальные связи W(2)-O (отмечены серым) на 3–8% короче, чем остальные четыре экваториальные связи (отмечены синим). Это говорит о том, что октаэдр одноосно сжат.
Подобное искажение, по словам ученых, сильно напоминает классический пример эффекта Яна — Теллера* в электронных системах t2g. В таком случае 5d-орбитали, лежащие в экваториальной плоскости, должны быть заняты электронами (2f).
Эффект Яна — Теллера* — возникает, когда взаимодействие между электронами и колебаниями ядер приводит к образованию локальных деформаций и изменению симметрии кристалла (статический эффект), или когда образуются вибронные состояния (динамический эффект).
Между занятыми 5d-орбиталями в малом треугольнике происходит значительное перекрытие через 2p-орбиталь O. А вот в большом треугольнике наблюдается небольшое перекрытие. Это указывает на то, что два электрона в трех атомах W(2) заключены в тримере W3 в маленьком треугольнике.
Для образования этого тримера электронная корреляция 5d электронов в CsW2O6 может быть еще одним существенным фактором. В тримере CsW2O6 два 5d электрона образуют спин-синглетную пару, что приводит к немагнитному и диэлектрическому основному состоянию. Таким образом мы наблюдаем альтернативный тип самоорганизации d-электронов, реализованный в сильно коррелированном 5d-оксиде.
Для более детального ознакомления с нюансами исследования рекомендую заглянуть в доклад ученых и дополнительные материалы к нему.
Эпилог
Результатом сего исследования стало обнаружение того, что тримеры правильного треугольника W3 образуются при переходе 215 K в β-пирохлоре оксида CsW2O6. Определить это удалось с помощью измерений структурных и электронных свойств монокристаллических образцов.
По сути, ученые обнаружили молекулы тривольфрама в монокристаллах CsW2O6, охлажденных до -58 °C. При комнатной температуре CsW2O6 является хорошим проводником, но при охлаждении становится диэлектриком.
Когда кристалл находится в состоянии проводника, молекулы вольфрама образуют трехмерные сети тетраэдрических пирамид, связанных по их углам, известных как структура пирохлора. А симметрически распределенные между молекулами электроны образуют их связь. Если же образец охладить, то электроны меняют свое положение, от чего появляется два типа атомов вольфрама, которые отличаются своей валентностью. Такие изменения приводят к искажению связи вольфрама с атомами кислорода, что приводит к более сжатой форме соединения.
В процессе всех этих пертурбаций атомы вольфрама с более низкой валентностью образуют маленькие и большие треугольники по бокам тетраэдров вольфрама, причем очень маленькие молекулы тривольфрама образуют маленькие треугольники. Три атома вольфрама, являющиеся вершинами этих треугольников, держатся друг друга за счет всего лишь двух электронов.
Ученые заявляют, что на данный момент CsW2O6 является единственным известным примером, где подобный формат связи (два электрона на три атома) проявляется как фазовый переход. В последующих работах авторы сего исследования намерены глубже изучить соединения с пирохлорными структурами, что позволит открыть новые материалы с крайне необычными свойствами.
Благодарю за внимание, оставайтесь любопытствующими и хорошей всем рабочей недели, ребята. 🙂
Немного рекламы
Спасибо, что остаётесь с нами. Вам нравятся наши статьи? Хотите видеть больше интересных материалов? Поддержите нас, оформив заказ или порекомендовав знакомым, облачные VPS для разработчиков от $4.99, уникальный аналог entry-level серверов, который был придуман нами для Вас: Вся правда о VPS (KVM) E5-2697 v3 (6 Cores) 10GB DDR4 480GB SSD 1Gbps от $19 или как правильно делить сервер? (доступны варианты с RAID1 и RAID10, до 24 ядер и до 40GB DDR4).
Dell R730xd в 2 раза дешевле в дата-центре Equinix Tier IV в Амстердаме? Только у нас 2 х Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 ТВ от $199 в Нидерландах! Dell R420 — 2x E5-2430 2.2Ghz 6C 128GB DDR3 2x960GB SSD 1Gbps 100TB — от $99! Читайте о том Как построить инфраструктуру корп. класса c применением серверов Dell R730xd Е5-2650 v4 стоимостью 9000 евро за копейки?


