Автор сообщества Фанерозой, биотехнолог, Людмила Хигерович.

На дворе двадцать первый век, стремительными темпами информационные технологии захватывают все больше сфер нашей жизни, включая науку. С каждым годом они все глубже проникают в различные отрасли науки, способствуя их развитию и порождая новые, смежные дисциплины. Таковой, например, является геномика.
Геномика — один из разделов генетики, однако много общего имеет с междисциплинарной биоинформатикой, разделяя с ней предмет и методы исследования. Но прежде, чем мы подробно рассмотрим саму геномику, окунемся в историю ее происхождения.
Точной даты рождения геномика не имеет. Однако ее появление относят к 1980-м годам, незадолго после открытия структуры ДНК и начала распространения методов секвенирования. Некоторые ученые, правда, все же указывают год рождения геномики — 1977, год полной расшифровки генома бактериофага Φ-X179.
Вероятно, тут стоит притормозить и добавить парочку словарных справок под спойлер. Не все наши читатели хорошо знакомы с терминами, а некоторые уже успели позабыть.
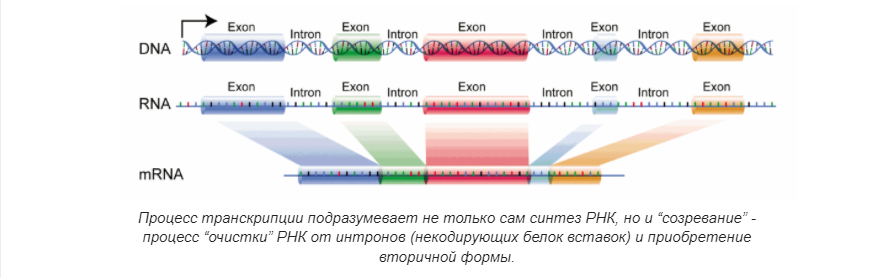
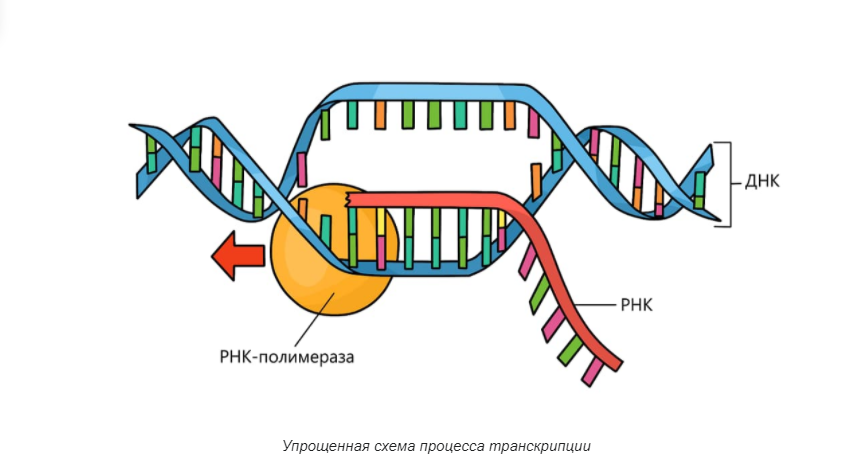
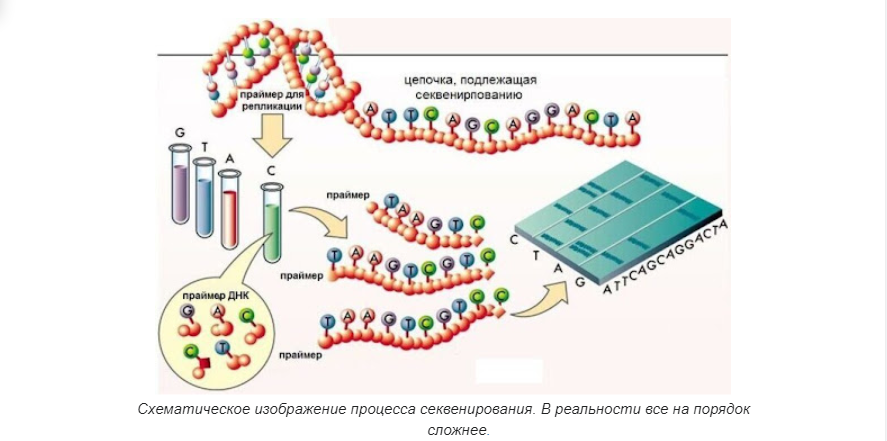
Повторение — мать учения. Итак, как мы говорили выше, геномика — это междисциплинарная область биологии, в которой основное внимание уделяется структуре, функциям, эволюции, картированию и редактированию геномов. Геном — это полный набор ДНК организма, включая все его гены, а также его иерархическую трехмерную структурную конфигурацию. В отличие от генетики, которая относится к изучению отдельных генов и их роли в наследовании, геномика направлена на коллективную характеристику и количественную оценку всех генов организма, их взаимосвязей и влияния на организм.
Почему геномика — важный раздел науки?
Гены могут управлять производством белков, с помощью ферментов и молекул-мессенджеров. В свою очередь, белки составляют структуры тела, такие как органы и ткани, а также контролируют химические реакции и передают сигналы между клетками. Геномика также включает в себя секвенирование и анализ геномов с использованием высокопроизводительного секвенирования ДНК и биоинформатики для сборки и анализа функции и структуры целых геномов. Достижения в области геномики вызвали революцию в исследованиях, основанных на открытиях, и в системной биологии, чтобы облегчить понимание даже самых сложных биологических систем, таких как мозг.
Эта область знаний также включает исследования внутригеномных (внутри генома) явлений, таких как эпистаз (влияние одного гена на другой), плейотропия (один ген влияет на более чем один признак), гетерозис (сила гибрида) и другие взаимодействия между локусами и аллелями внутри генома.

Чем больше люди изучали генетический аппарат живых организмов, тем становилось яснее, что усилий одного только человеческого мозга недостаточно для полноценного анализа и расшифровки. Так что как только появилась возможность машинного анализа, биологи с радостью поручили часть своей работы компьютерам. Так зародилась другая междисциплинарная область знаний — биоинформатика.
Биоинформатика — часть науки, объединяющая в себе генетику, биохимию и молекулярную биологию, математическую статистику и отчасти задевающую краем эволюционную и популяционную биологии, медицину и математическую статистику. Биоинформатики является междисциплинарным полем, которое разрабатывает методы и программные средства для понимания биологических данных, в частности, когда наборы данных являются большими и сложными. Как междисциплинарная область науки, биоинформатика сочетает в себе биологию, информатику, информационную инженерию, математику.и статистика для анализа и интерпретации биологических данных. Биоинформатика использовалась для анализа in silico (на компьютере) биологических запросов с использованием математических и статистических методов.
Некоторые соотносят биоинформатику с геномикой, однако они не перекрывают друг друга полностью — скорее, геномика пользуется достижениями биоинформатики, и в то же время сама является инструментом ее пополнения и расширения.
Разделы геномики
За почти пятьдесят лет своего существования геномика значительно расширилась и приобрела внутреннюю структуру — разделилась на несколько направлений, тем не менее, все еще зависящих друг от друга. Деление это весьма условно, многие отделы не просто пересекаются, а значительно перекрывают друг друга.

Геномику подразделяют на следующие направления:
- Структурная геномика
- Функциональная геномика
- Сравнительная геномика
- Музеогеномика
- Когнитивная геномика
- Вычислительная геномика
Структурная геномика — самый крупный и самый “развитый” раздел. Ее задача — выяснение конечной структуры белка, закодированного в исследуемой последовательности. Это важно при расшифровке генетической информации: мало выяснить, какие основания и как расположены в участке ДНК, гораздо более интересно, во что она транскрибируется.
И этот интерес отнюдь не праздный — состав и структура белка могут многое сказать о его функции и месте в метаболизме.

После синтеза аминокислотная цепочка (первичная структура) “плавает” в цитоплазме, и сворачивается в петли. Когда подходящие участки белка сближаются, в дело вступают молекулярные химические силы — некоторые места “слипаются” под действием сил водородных связей, ионных связей, а также сил Ван-дер-Ваальса, образуя вторичную объемную структуру — альфа-спираль и бета-лист. На этом их преобразование не останавливается — в конечном итоге белок приобретает форму глобулы — плотно свернутого клубка. В таком виде он обычно и существует, выполняя свои функции.
Знание третичной структуры позволяет сделать предположение о функциях белка — это не просто комок аминокислот, глобула устроена так, что у нее есть домены — участки с разным предназначением. Условно их делят на основную часть и функциональную — например, ферментирующая ямка (энзимы и пищеварительные ферменты), “хвост” для закрепления на мембране (кинезины, мембранные белки), участки, “примагничивающиеся” к другим белкам (актино-миозиновый комплекс в мышцах) и т. д.
Этому даже посвящен значительный раздел биоинформатики — он так и называется, предсказание структуры белка (protein structure prediction). Это преимущественно математическое моделирование с опорой на молекулярную биологию и химию. Помимо расшифровки первичной структуры, необходимо учитывать две важные вещи — количество свободной энергии и нахождение глобального минимума энергии. Это звучит, как магическая формула, однако на практике это то, от чего зависит, как и насколько преобразуется и свернется белок. Кроме того, требуются огромные вычислительные мощности для расчета всех возможных вариантов пространственной структурой белка — а это миллионы вариантов для белка длиной в сотню аминокислотных остатков. Круг поиска несколько сужают методы предсказания укладки (альфа-спираль или бета-лист, и участки с повышенной вероятностью “слипания”) и гомологическое (сравнительное) моделирование, основанное на знании о структуре хорошо изученных белков. В то же время его осложняют возможные посттранскрипционные преобразования — белок не просто меняет свою пространственную структуру, но также может распадаться, разрезаться ферментами, сшиваться и приобретать конечные свойства только в четвертичной структуре — в комплексе с другим белком.
Помимо этого, структурная геномика в комплексе с функциональной может предсказывать болезни, возникающие при генетических аномалиях. Так, было выяснено, что мутация в одном из белков мембраны клеток может вызывать иммунитет организма к ВИЧ СПИДу, но при этом ослабляет его перед ОРВИ и лихорадкой западного Нила. Этот же белок отчасти ответственен за тип вашего темперамента — гипертимный ли, флегматичный и т. д. Эта часть соотносится с функциональной геномикой.

Функциональная геномика своей основной задачей ставит прослеживание полного пути реализации генома. Она показывает, как определенный ген превращается в белок, и какой конечный признак в организме от него зависит, чем приближается к протеомике — междисциплинарной отрасли науки, изучающей структуру и функции протеинов и белков в частности. Это весьма сложно в рамках многоклеточного организма, так как один и тот же белок выполняет множество функций. Кроме того, разные белки могут одновременно влиять на один и тот же признак.
Так, например, цвет глаз человека кодируют как минимум 6-8 генов на 2-3 хромосомах. За светлые глаза в основном отвечает мутация гена OCA2. За синий или зелёный цвет отвечает ген EYCL1 хромосомы 19; за коричневый — EYCL2; за коричневый или синий — EYCL3 хромосомы 15. Кроме того, с цветом глаз связаны гены OCA2, SLC24A4, TYR, влияющие на оттенки и переходные цвета. Все эти гены, вернее, их белки, действуют одновременно, благодаря чему найти два одинаковых рисунка радужки почти невозможно. Кроме того, в зависимости от перенесенных заболеваний, питания и выцветания на солнце цвет глаз меняется в течении всей жизни, что еще больше осложняет работу по составлению статистических исследований.
Сравнительная геномика близка к эволюционной биологии и популяционной генетике. Она сравнивает организацию и функционирование генома у разных систематических групп организмов, изучает их принципиальные сходства и различия, и ищет аналогию между ними. Значительную часть составляет поиск гомологий и аналогий у разных организмов с геномом человека — вопрос больше практический, чем праздный. От этого зависит выбор организма для производства лекарственных средств или даже выращивания органов и тканей для трансплантации. Так, многие фармацевтические препараты, а также витамины производят с помощью бактерий, так как их генетический аппарат почти не преобразует конечный продукт, и при этом обладает достаточным функционалом для синтеза. Ну и, конечно, их относительно легко модифицировать и культивировать.
Музеогеномика — во многом схожа со сравнительной. Только специализируется на исследовании генома музейных экспонатов — палеонтологических, зоологических, ботанических и других. Она позволяет установить степень родства вымерших таксономических групп, проследить эволюцию признака у ископаемых растений и даже предположить, какие животные были предыдущими носителями вирусов и прочих паразитов. Кроме того, музеогеномика позволяет проследить токсигенное влияние человека, сравнивая образцы столетней давности с сегодняшними обитателями Земли.

Когнитивная геномика. Несколько странное направление в контексте современных исследований. Казалось бы, человечество еще в прошлом веке пережило предрассудки о наследовании характера и умственных способностей и связи этого с внешностью. Однако полностью отрицать влияние генетики на мозговую активность — тоже неправильно. Белковый состав мембран нервных клеток, а также степень и качество миелинизации (образования изолирующих оболочек) оказывает сильное влияние на тип нервной системы и темперамент.
Темперамент человека зависит от типа нервной системы, что в свою очередь зависит от состава и количества мембранных белков, структура которых закодирована в ДНК — по оценке Вайнбергера, примерно 70% всех генов организма оказывает влияние на нервную систему, в частности на головной мозг. С возрастом, разумеется, на темперамент оказывает влияние опыт, физиологические преобразования и воспитание, что формирует вторичные структуры — характер и личность. Однако базовые параметры так или иначе заложены генетически.
В рамках когнитивной отлично уживаются элементы сравнительной геномики. Ученые сравнивают геномы нескольких видов, чтобы выявить генетические и фенотипические различия между ними. Наблюдаемые фенотипические характеристики, связанные с высшей нервной деятельностью, включают поведение, личность, нейроанатомию и невропатологию. Теория когнитивной геномики основана на элементах генетики, эволюционной биологии, молекулярной биологии, когнитивной психологии, поведенческой психологии и нейрофизиологии.
Но когнитивная геномика не ставит своей задачей узнать, кто родился с большим шансом стать гением, а кто с меньшим. В первую очередь когнитивная геномика работает с выявлением причин патологий высшей нервной деятельности и аномалий мозга, а также исследует возможные способы их лечения или уменьшения. Большинство поведенческих или патологических фенотипов происходят не из-за мутации только одного гена, а из-за сложной генетической основы. Однако есть некоторые исключения из этого правила, такие как болезнь Гентингтона, которая вызвана одним конкретным генетическим заболеванием. На возникновение нейроповеденческих расстройств влияет целый ряд факторов, генетических и негенетических. Методы когнитивной геномики были использованы для изучения генетических причин многих психических и нейродегенеративных расстройств, включая синдром Дауна, большое депрессивное расстройство, аутизм и болезнь Альцгеймера.
Вычислительная геномика — самая близкая к биоинформатике часть, родившаяся и развивающаяся одновременно с ней. Так или иначе, ее элементы используют все остальные разделы геномики. Ее основа — вычислительный анализ, позволяющий расшифровать не только отдельные участки или гены, но охватить геном целиком, включая не только последовательность нуклеотидов в ДНК, но и синтезированную на ее основе РНК.
Геномика и Big Data
Геном даже одного простейшего организма состоит из тысяч или даже десятков тысяч пар оснований. Анализ одной только цепочки ДНК из одной хромосомы “вручную” занимает годы, если не десятилетия. Прибавим к этому то, что секвенирование зачастую предполагает разрезание ДНК на маленькие кусочки, и получим еще одну задачку — собрать расшифрованные кусочки в нужном порядке. Эта задача, называемая генетическим картированием, поистине титаническая. И хоть без человеческого умственного труда все равно не обойтись при финальном сведении данных и написании вывода, то значительную часть аналитического труда выполняет компьютер.
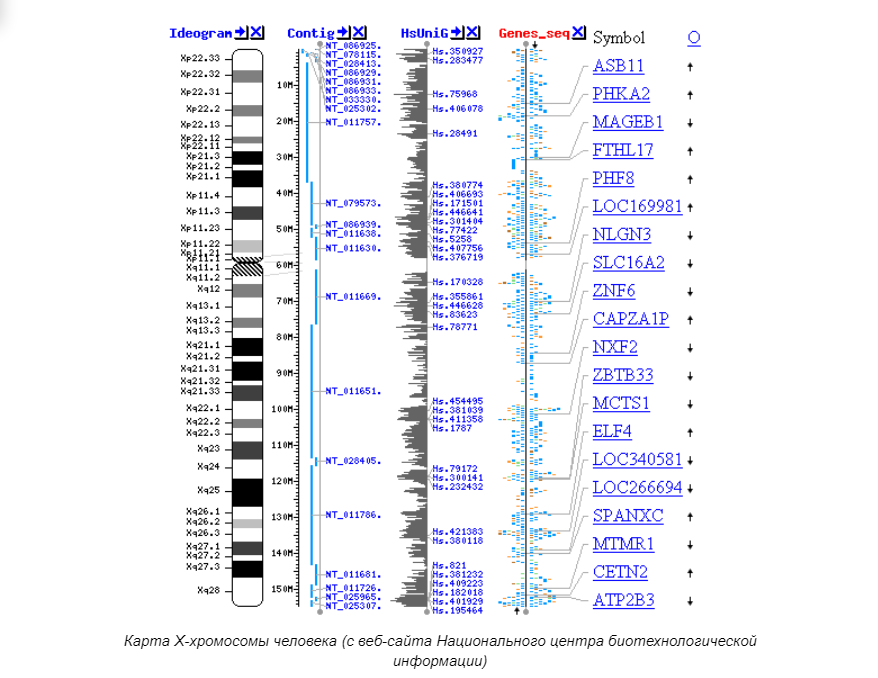
Специально для целей геномики даже были разработаны особые программные и иерархические средства анализа. Так, например, были разработаны специфические «конвейеры» анализа, неоднократно “прогоняющие” одну и ту же последовательность, а затем повторяющие эти же процедуры с другой, в конечном итоге сравнивая полученные результаты и фиксируя сходства и различия. Обычно это используется для идентификации генов-кандидатов (изменения в них могут вызвать онкологию) и однонуклеотидных полиморфизмов (точечных мутаций, характеризующихся многократным, идущим подряд повторением основания на одной из цепей, что вызывает разрыв между цепями).
Компьютерный анализ также помогает при аннотировании — маркировании генов. Этот процесс необходимо автоматизировать, потому что большинство геномов слишком велики для аннотирования вручную, не говоря уже о необходимости аннотировать как можно больше геномов, поскольку скорость секвенирования перестала быть проблемой. Аннотации стали возможными благодаря тому факту, что гены имеют узнаваемые начальные и конечные области (промоторы и терминаторы, имеющие зачастую схожий или одинаковый состав у разных групп организмов), хотя точная последовательность, обнаруженная в этих областях, может варьироваться между генами.
Кроме аннотирования и анализа отдельного генома, технологии Big data позволяют массово сравнивать геномы особей в популяциях и даже видов. Так появилась, например, вычислительная эволюционная биология. Эволюционная биология — это изучение происхождения и происхождения видов, а также их изменения с течением времени. Информатика помогла эволюционным биологам, позволив исследователям:
- Отслеживать эволюцию большого числа организмов, измеряя изменения в их ДНК, а не только с помощью физической систематики или физиологических наблюдений
- Сравнивать целые геномы, что позволяет изучать более сложные эволюционные события, такие как дупликация генов, горизонтальный перенос генов, а также предсказывать факторы, важные для видообразования бактерий
- Построение сложных вычислительных моделей популяционной генетики для прогнозирования результатов работы системы с течением времени
- Отслеживать и обмениваться информацией о все большем количестве видов и организмов.
В перспективе это поможет составить более подробное и правдоподобное филогенетическое дерево — т. н. древо жизни, отражающее примерную эволюцию живого.

Такие сложности возникают потому, что в процессе эволюции ДНК не только усложняется, но и упрощается, теряя “ненужные” участки в ходе делеций или отбора. Кроме того, существует такое явление, как горизонтальный перенос генов — обмен участками генома между генетически неродственными группами. Так, например, значительная часть интронов у бактерий, растений и животных, включая человека, — это следы заражения вирусами, которые потеряли часть своего генома, ответственную за синтез оболочки вируса и репликацию.
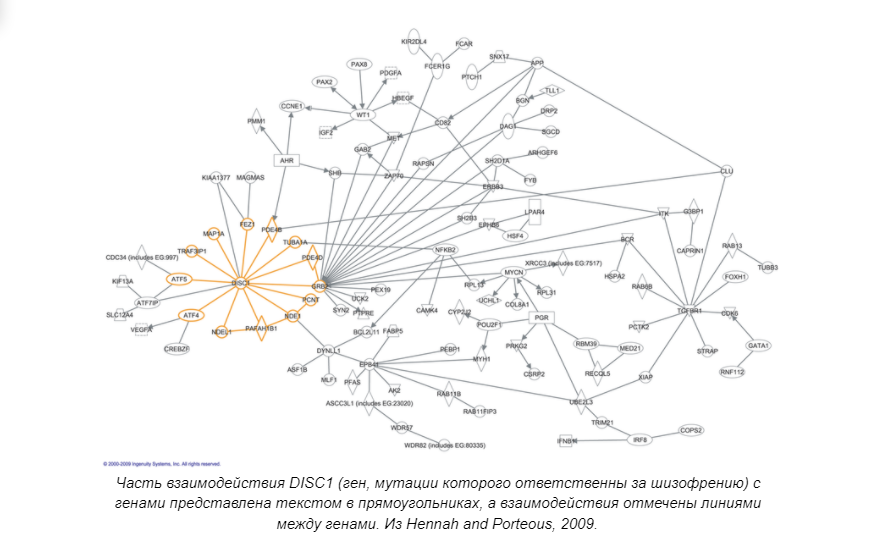
В рамках вычислительной геномики существует также такое понятие, как Интерактом (Interactome) или сети молекулярного взаимодействия. В двух словах, это совокупность локализаций и взаимодействий конкретной молекулы в рамках одной конкретной клетки. Такая модель также может описывать наборы непрямых взаимодействий между генами. Молекулярные взаимодействия могут происходить между молекулами, принадлежащими к разным биохимическим семействам (белки, нуклеиновые кислоты, липиды, углеводы и т. д.), а также внутри каждого семейства. Когда такие молекулы связаны физическими взаимодействиями, они образуют сети молекулярных взаимодействий, которые обычно классифицируются по природе задействованных соединений. Чаще всего, интерактом относится к сети межбелкового взаимодействия (PPI) (PIN) или ее разновидностям.
Это чрезвычайно сложная схема, реализация которой была бы невозможна без компьютерного моделирования. Она настолько сложна технически и важна практически, что в последнее время выделяется в самостоятельную область биоинформатики.
Биоинформатика для всех
Помимо решения сложных узкопрофильных задач, для которых обычно создаются специальные программные методы, существуют и более широкого спектра сервисы.
Так, есть ряд проектов, призванных помочь любому желающему провести быстрый анализ полученного сиквенса или белка — рано или поздно с такой проблемой сталкивается любой биолог-исследователь.
Первым подобным проектом стал алгоритм Нидлмана — Вунша на основе динамического программирования. Он был создан для того, чтобы сравнить наборы последовательностей аминокислот друг с другом при использовании матриц замен, полученных в более раннем исследовании М. Дейхофф.

Позже появился алгоритм BLAST, который позволяет осуществлять быстрый и оптимизированный поиск в базах данных последовательностей генов. BLAST и его модификации — одни из наиболее широко используемых алгоритмов для этой цели.
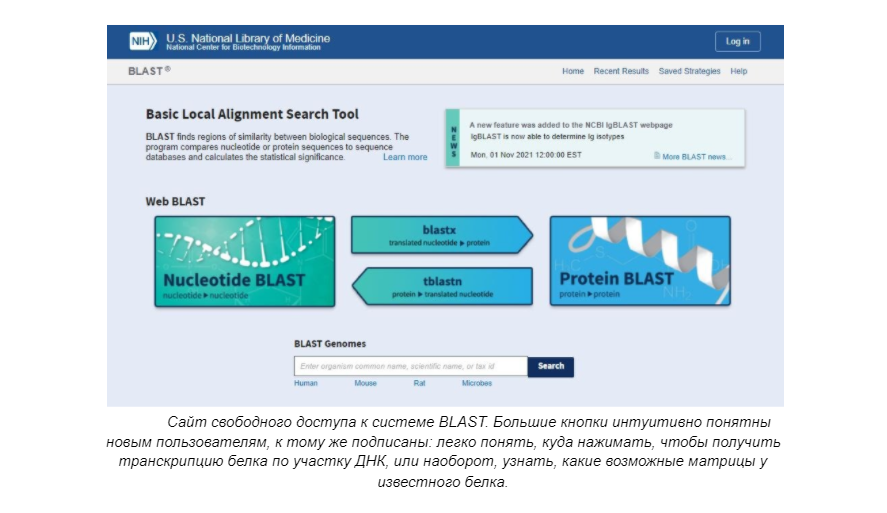
Примерно теми же функциями обладают и системы UGENE и DNAStar, однако пользование ими для обычного человека затруднено, к тому же есть платные пакеты с расширенным функционалом. Кроме того, существуют различные сервисы по моделированию возможной структуры белков. Таковым является, например, Google DeepMind.
На этом мы завершим очередную мини-экскурсию в мир биологической информатики или информативной биологии. Надеемся, что вы сегодня узнали что-то новое и интересное.
Всего хорошего и не болейте!
Lesk AM (2017). Introduction to Genomics (3rd ed.). New York: Oxford University Press. p. 544.
Dong Xu, Lukasz Jaroszewski, Zhanwen Li, Adam Godzik. AIDA: ab initio domain assembly for automated multi-domain protein structure prediction and domain–domain interaction prediction (англ.) // Bioinformatics. — 2015-07-01. — Vol. 31, iss. 13. — P. 2098—2105.
Plomin, R. & Spinath, F.M. (2004). «Intelligence: Genetics, Genes, and Genomics.» Journal of Personality and Social Psychology, 86(1): 112—129
.
Sulem P., Gudbjartsson D. F., Stacey S. N., et al. Genetic determinants of hair, eye and skin pigmentation in Europeans (англ.) // Nat. Genet.: journal. — 2007. — December (vol. 39, no. 12). — P. 1443—1452.
Blue Eyes Versus Brown Eyes: A Primer on Eye Color Архивировано 8 декабря 2012 года… Eyedoctorguide.com. Retrieved on 2011-12-23.
Gonnet G. H. 2012. Surprising results on phylogenetic tree building methods based on molecular sequences. BMC Bioinformatics, 13:148
Google’s DeepMind predicts 3D shapes of proteins, The Guardian. 2018
Hug, L., Baker, B., Anantharaman, K. et al. A new view of the tree of life. Nat Microbiol 1, 16048 (2016).
Julian Vosseberg, Jolien J. E. van Hooff, Marina Marcet-Houben, Anne van Vlimmeren, Leny M. van Wijk, Toni Gabaldón & Berend Snel. Timing the origin of eukaryotic cellular complexity with ancient duplications // Nature Ecology and Evolution. 2020. DOI: 10.1038/s41559-020-01320-z.
Papanikolaou, N.; Pavlopoulos, G.A.; Theodosiou, T.; Iliopoulos, I. Protein-protein interaction predictions using text mining methods (англ.) // Methods: journal. — 2015. — Vol. 74. — P. 47—53.
Mikhail Fursov, Olga Golosova, Konstantin Okonechnikov. Unipro UGENE: a unified bioinformatics toolkit (англ.) // Bioinformatics. — 2012-04-15. — Vol. 28, iss. 8. — P. 1166—1167.
Wang L, Eftekhari P, Schachner D, Ignatova ID, Palme V, Schilcher N, Ladurner A, Heiss EH, Stangl H, Dirsch VM, Atanasov AG. Novel interactomics approach identifies ABCA1 as direct target of evodiamine, which increases macrophage cholesterol efflux. Sci Rep. 2018 Jul 23;8(1):11061.
Kotlyar M, Pastrello C, Pivetta F, Lo Sardo A, Cumbaa C, Li H, Naranian T, Niu Y, Ding Z, Vafaee F, Broackes-Carter F, Petschnigg J, Mills GB, Jurisicova A, Stagljar I, Maestro R, Jurisica I (2015). «In silico prediction of physical protein interactions and characterization of interactome orphans». Nature Methods. 12 (1): 79–84.
Robson JF, Barker D (October 2015). «Comparison of the protein-coding gene content of Chlamydia trachomatis and Protochlamydia amoebophila using a Raspberry Pi computer». BMC Research Notes. 8 (561): 561.
Dawson WK, Maciejczyk M, Jankowska EJ, Bujnicki JM (July 2016). «Coarse-grained modeling of RNA 3D structure». Methods. 103: 138–56.



