
После своего возникновения Земля представляла знойную и горячую сферу без жизни. Спустя же 4,5 миллиарда лет фауна и флора оказались представлены многочисленными формами ныне живущих организмов, продолжающих эволюционировать на молекулярном уровне. В этой работе мы с вами попытаемся проникнуть через тектонические плиты истории, слой за слоем углубимся к описанию первоначальных алгоритмов химических реакций и ответим на вопрос: «Где, в каком количестве и из чего возникли сложные органические молекулы, прошедшие долгий путь эволюции в живые существа?». Чтобы обуздать порядок эволюционного отбора, понадобится прочный фундамент теории, для дальнейшей логистики рассуждений и статистических описаний.
Пролог: структура и организация носителей информации
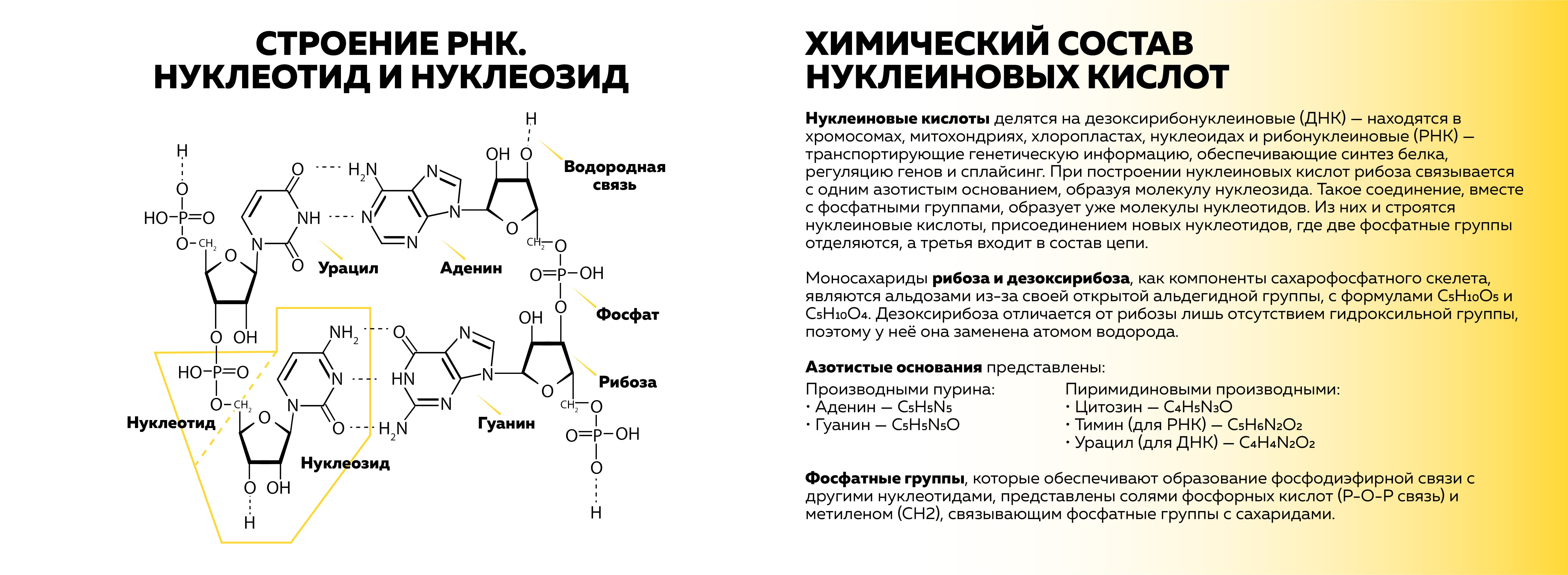
Прежде чем перейти к химическим реакциям получения органических соединений, мы изучим молекулы, условия абиогенного синтеза которых будем искать большую часть статьи. Нуклеиновые кислоты делятся на дезоксирибонуклеиновые (ДНК) — находятся в хромосомах, митохондриях, хлоропластах, нуклеоидах и рибонуклеиновые (РНК) — транспортирующие генетическую информацию, обеспечивающие синтез белка, регуляцию генов и сплайсинг. При построении нуклеиновых кислот рибоза связывается с одним азотистым основанием, образуя молекулу нуклеозида. Такое соединение, вместе с фосфатными группами, образует уже молекулы нуклеотидов (рис. 1). Из них и строятся нуклеиновые кислоты присоединением новых нуклеотидов, где две фосфатные группы отделяются, а третья входит в состав цепи [3].
Моносахариды рибоза и дезоксирибоза, как компоненты сахарофосфатного скелета, являются альдозами из-за своей открытой альдегидной группы, с формулами С5H10O5 и С5H10O4. Дезоксирибоза отличается от рибозы лишь отсутствием гидроксильной группы, поэтому у неё она заменена атомом водорода.
|
Производные пурина: |
Пиримидиновые производные: |
|
Аденин — C5H5N5 |
Цитозин — C4H5N3O |
|
Гуанин — C5H5N5O |
Тимин (для РНК) — C5H6N2O2 |
|
Урацил (для ДНК) — C4H4N2O2 |
Таблица 1. Азотистые основания
Фосфатные группы, которые обеспечивают образование фосфодиэфирной связи с другими нуклеотидами, представлены солями фосфорных кислот (P-O-P связь) и метиленом (СН2), связывающим фосфатные группы с сахаридами.
Введение: химический состав архея
В начале своего формирования, около 4 миллиардов лет назад, атмосфера планеты пополнялась лишь газами, исходящими из расплавленных геологических структур. При движении магмы в ядре магнитное поле благоприятствовало осаждению карбонатов и сдерживало целостность атмосферы [1]. Барьер из озона, образовавшийся в процессе реакции действия ультрафиолета (фотолиза), создал нужный тепловой баланс к концу архейского эона [2]. В этот период, в атмосфере содержались:
-
Водород (Н2)
-
Метан (СН4)
-
Аммиак (NH3)
-
Азот (N2)
-
Диоксид углерода (СО2)
-
Монооксид углерода (CO)
-
Вода (Н2O)
-
Сероводород* (Н2S)
-
Диоксид серы* (SO2)
*В атмосфере соединение серы неустойчивы, но при поступлении из глубин, содержание сохраняется.
Введение: первые алгоритмы синтеза — первые проблемы
В начале XX века А. Опарин и Д. Холдейн работали над концепцией коацервата. Их интересовало то, каким образом синтезируется сложная органика при разрядах молний, ультрафиолета и извержений вулканов [4]. Идея частично подтвердилась Г. Юри и С. Миллером. Смесь соединений, имитирующих древнюю атмосферу, запаивалась в замкнутой установке и в колбу с водой пропускали электрический ток. Спустя две недели, на протяжении которых им периодически приходилось наблюдать за реакциями через стекло, они вскрыли колбу и выяснили, что теперь в ней присутствовали аминокислоты, сахара и органические кислоты [5]. Эксперимент показал реальность синтеза сложной органики из более простых химических веществ.
-
CO2 → CO + [O] (атомарный кислород)
-
CH4 + 2[O] → CH2O (формальдегид) + H2O
-
CH4 + NH3 → HCN (синильная кислота) + 3H2
Полученные в вышеописанных реакциях соединения формальдегида, синильной кислоты и аммиака, синтезируют аминокислоты в процессе реакции Штрекера, а вода и формальдегид — рибозу, в процессе реакции Бутлерова. Последующие эксперименты синтезировали производные пурина (таблица 1) и расширили список получаемых аминокислот. Казалось бы, вот же переход от химической эволюции к биологической. Но как это бывает, бронежилет теории не выдерживает обстрела реальности — концепция коацервата имела серьёзные недостатки. Реакция соединения аминокислот в белок или нуклеотиды происходит с выделением воды, и длинные молекулы подвержены распаду [1]. Ещё одной проблемой стал способ размещения вокруг атома углерода связей, которые являются взаимно-зеркальными — хиральными [6]. Аминокислоты чаще представлены левыми изомерами, а рибозы — правыми. Такая характеристика нуклеотидов придаёт спиральную структуру ДНК и РНК, но в синтезе из простых соединений получается равное количество изомеров, поэтому белки такой смеси не способны функционировать.
Теория условий: источники условий для концентрации
Высокое содержание железа, цинка, марганца и меди — особенность живых клеток. Если железа много в неживой природе, то меди с марганцем и цинком — не особенно. Парадоксально, но все они содержатся в клетках в намного большей концентрации, чем во внешней среде. Перечисленные металлы характерны в обильном количестве для гидротермальных источников, с которых мы начнём поиск условий для абиогенного синтеза органических соединений.
Воды источников имеют чёрный цвет благодаря сульфидам, сероводороду и другими взвесям [10]. После контакта с океаном гидротермальные воды охлаждаются, а соединения железа, меди и никеля выпадают в осадок. При дальнейшем остывании вод сульфиды цинка и марганца осаждаются на уже сформированный рельеф.
Сульфиды цинка способны к фотохимическому восстановлению, поглощая ультрафиолет и фосфоресцируя. В таком состоянии возбуждённый электрон восстанавливает соединения диоксида углерода до муравьиной и других органических кислот, а при ультрафиолете восстанавливает азот до аммиака. При этом он защищает органические молекулы от ультрафиолета эффективней слоя воды в десятки метров. Именно поэтому первые организмы могли укрываться в минеральных осадках, имея доступ к продуктам фотохимических реакций [1].
Осадки образуются из мелких частиц и имеют много пор. Подобные условия являются удобными для репликации органики из-за относительной изоляции. Откладывающиеся сульфидные минералы становятся катализаторами химических реакций для синтеза органических соединений [11]. Градиенты температур разделяют хиральные формы соединений. В таких условиях термодиффузии РНК и белки накапливаются в одной локации, например — в вышеупомянутых порах, где происходит концентрация в миллиарды раз [12].
Теория условий: количественные исследования синтеза
Важным веществом клетки является фосфор, содержащийся в фосфорилированных органических молекулах, входящих в состав нуклеиновых кислот, аденозинтрифосфатов и др. Источниками достаточного количества этого вещества являются вулканы и горячие геотермальные источники. Они содержат фосфиты, пирофосфаты, или оксиды фосфора. При растворении эти соединения дают молекулы в пригодной для сахарофосфатов и нуклеотидов форме. В условиях кипения минеральных вод растворённые соединения разделяются, поэтому часть испаряется с водой и выходит в грязевых котлах. В виду подобной сепарации металлов поднимающийся пар магмы содержит бораты, калий, натрий и соли молибдена в концентрации такой же, как в органической клетке.
Проводились исследования с использованием солей бора, где образовывались комплексы 5/6-углеродных сахаров, выпадающие в осадок, и происходило накопление молекул с двумя соседними гидроксильными группами. При добавлении гидроксиапатита в такую смесь на его поверхности откладывается рибоза [18][19], а соли молибдена превращают разветвлённые сахара в линейные, увеличивая синтез. Почувствуйте, как густые и горячие знания стекают вам на шею, ведь грязевые котлы обогащены всеми вышеописанными ранее элементами [15], потому и представляются одними из самых вероятных мест появления жизни, имея несколько преимуществ сразу:
-
Условия, богатые необходимыми микроэлементами;
-
Источник тепла с постоянными условиями;
-
Пористые минеральные осадки, работающие в качестве катализаторов и локации для репликации органических соединений;
-
Испарение на местах при концентрации веществ, солей и кислот, где происходит образование цепочек РНК;
-
Несколько путей получения органических молекул;
-
Фотохимические реакции и расположенные рядом защищённые поры;
-
Нагрев пор, где накапливаются нуклеотиды и РНК в высоких концентрациях.
Теория условий: лаборатория Манчестера — анализ системы синтеза
В 2008 году вышло исследование об обнаруженных на дне океана колонн из светлого известняка высотой до 60 метров. Из их недр исходила вода температурой около 80°С и содержала соединение гидроксида магния, выпадающее в осадок. Нагрев происходил за счёт реакций в глубине твёрдых пород, поэтому метан и кислоты этих вод образуются абиогенно, а изотопный состав углерода в них такой же, как в углекислом газе [16]. В атмосфере древнего мира метан реагировал с азотом, водой и углекислым газом, образуя формальдегид. Соединения фотолиза метана не накапливались, а выпадали с дождём (рис. 2). Синильная кислота и формальдегид растворимы в воде, поэтому они вымывались и на поверхность поступали формальдегид, цианамид и цианид — являющиеся прекурсорами для азотистых оснований и РНК [17].

Реакция получения нуклеотидов с помощью таких соединений была получена в 2009 году в Манчестере, во время работы Д. Сазерленда и его коллег [20]. Они синтезировали пиримидиновые нуклеотиды путём смешения в одной установке предшественников сахаров и нуклеотидов с фосфатами (рис. 3).
Сейчас придётся хрустеть коркой головного мозга, но чтобы было проще, обратимся к рисунку 3 ниже, который будет иллюстрировать ход реакций. Как можем видеть, первоначальные соединения представлены: цианоацетиленом, цианамидом, глицеральдегидом и гликольальдегидом.

Фосфат в реакции не только облегчает синтез нуклеотидов, подавляя побочные реакции, но и направляет соединение цианамида с гликольальдегидом в сторону аминооксазола. А уже его соединение с глицеральдегидом образует арабинозо-аминооксазолин. В реакции же аминооксазолина с цианоацетиленом снова фосфат помогает реакции — он поддерживает кислотность и создаёт условия для получения арабинозо-ангидронуклеозида.
После, достаточно подогреть реакционную смесь для получения циклического цитидин-монофосфата. Такой раствор освещается ультрафиолетом, чтобы превратить часть цитозина в урацил и избавиться от побочных продуктов. Аналогичным способом получены пуриновые нуклеотиды при добавлении синильной кислоты вместо цианоацетилена. Всего из четырёх простых соединений получаются все нуклеотиды и десять из двадцати белковых аминокислот. Но главное, в реакциях почти не образуется соединений, не встречающихся в клетках. Этот момент станет сюжетной пружиной повествования.
РНК: эволюция информации с помощью репликаторов
В конце XX века произошло открытие рибозимов. До того времени РНК считалась только связующим элементом ДНК и белков, но последующие исследования показали способность РНК заменять белки в качестве катализаторов реакций, а также их ключевое значение в организации синтеза белка. Появилась гипотеза «РНК мира». Согласно этой теории, реплицирующиеся рибозимы стали первыми органическими соединениями, начавшими эволюцию. Спустя поколения репликаторы предоставили каталитические функции белкам, а хранение генома практически полностью — ДНК [7]. Однако без клеточных систем получение полноценных белков в водной среде невозможно. Вопрос решается нахождением условий, где участие воды в реакции снижено или у неё отсутствуют химически свободные молекулы — благо, примеры таких локаций мы уже с вами рассмотрели в предыдущих главах.
РНК: алгоритм отбора палиндромных молекул
Двигаемся дальше. В условиях липидно-нуклеотидного раствора уже рассмотренных грязевых котлов образуются последовательности РНК в 50-100 нуклеотидов. Липиды, к которым мы вернёмся позже, при высыхании образуют слои и длинные цилиндры, где последовательности РНК упорядоченно накапливаются и сохраняют подвижность. При естественном отборе преимущество получают те последовательности, которые служат фрагментами для создания собственных копий — палиндромные цепи РНК [21]. Эта идея А. Маркова превращает необходимость фрагментов в фактор естественного отбора, который может привести к образованию рибозима среди длинных палиндромных молекул. Это частично подтверждает геноцентричный взгляд на эволюцию Ричарда Докинза [22], ведь палиндромный способ упаковки молекул наблюдается и в последовательностях соединений нынешних транспортных РНК.
Устойчивость к ультрафиолету тоже может быть признаком отбора, при котором выживали более длинные цепи. В таких молекулах защита соседних соединений осуществлялась за счет параллельных связей азотистых оснований — стэкинг-взаимодействия, похожего на «слоёный пирог» [9]. Важно то, что увеличение количества собственных копий способствует не только копированию, но и превращению простых органических веществ в нуклеотиды. В совокупности, это знаменует появление обмена веществ, где реакции происходят при контроле ферментов.
РНК: вещественный обмен
Обмен веществ у первых органических структур развивался гетеротрофно, от сложных исходных соединений, как рибоза и азотистые основания, к более простым [1]. На начальных этапах РНК были доступны многие активные одноуглеродные соединения:
-
Муравьиная кислота образуется при фотосинтезе на сульфиде цинка и выносится геотермальными источниками после реакций воды с базальтами.
-
Формальдегид опадает с дождями, возникая при фотолизе метана.
-
Угарный газ выделяется в составе газов вулкана.
Все три случая рассмотрены ранее и внимательный читатель вспомнит их, но именно диоксид углерода стал конечным нужным соединением. Хотя его восстановление без качественных катализаторов медленное, мы помним, что при абиогенном восстановлении реакция происходит под действием ультрафиолета или температуры. Выбор между способами использования углерода в обмене веществ зависит от среды. Рибулозо-монофосфатный цикл питаемый формальдегидом [23] похож на древнейший синтез сахаров, а участие муравьиной кислоты в синтезе пуринов (таблица 1), предполагает формирование этой реакции до появления ферментов фиксации диоксида углерода.
РНК: энергия липидной мембраны
Возвратимся к теме липидов. Электроны связей молекулы воды смещены из-за большей электроотрицательности кислорода. Вследствие этого, одна сторона молекулы несёт положительный заряд, а другая — отрицательный [27]. Поэтому вещества с полярными молекулами (гидрофильные) притягиваются и смешиваются с водой, а неполярные молекулы (гидрофобные) — нет [28]. В живых организмах клетки окружены мембраной из двух слоёв липидов, при смешивании их молекул в воде получается эмульсионная взвесь, а не растворение [29]. Наружная сторона мембраны несёт положительный заряд, а внутренняя — отрицательный. Такой электрический потенциал используется при передаче и хранении энергии, а также транспорта веществ вместе с протонами для компенсации заряда мембраны [30][31].
Вероятно, протоклетки имели примитивные оболочки из липидов, которые пропускали протоны и ионы металлов, но задерживали белки и РНК, поэтому выход из геотермальных водоёмов в среду с высоким содержанием натрия потребовал создания клетками способа его «откачки» [32]. Появления натриевых насосов использующих энергию реакций и освоение новых кислых сред, подтверждает образование мембран в тот период, когда аденозинтрифосфаты уже были в наличии.
Эволюция РНК: кластеризация вирусов
Каким всё-таки образом ДНК сменила функцию РНК в хранении генома? Реакция превращения рибозы в дезоксирибозу связана с образованием опасных радикалов, поэтому рибозимы не могут её осуществлять. Реакцию проводят ферменты — большие белки, для кодирования которых нужны минимум тысячи нуклеотидов. Между теперешним способом хранения нуклеиновых кислот и миром РНК, были промежуточные формы более простые в получении чем ДНК, но стабильнее РНК [7]. Эволюция предковых образований клеток тесно связана с вирусами. Так, П. Фортер считает главной стадией жизни вируса — её активную часть в заражённой клетке [24]. Вирусы образуют кластеры сочетающие клеточные и вирусные белки, где клетки синтезируют копии вируса при контроле вирусного генома.
На этом этапе видно, что задача хранения генетической информации осуществляется разными вариациями соединений, но естественным отбором избраны содержащиеся в нынешних клетках. К слову, синтетическая биология достигла больших результатов, создавая альтернативные нуклеотиды. В 2014 году «нуклеотидный алфавит» был расширен до шести букв за счет включения нескольких синтетических пар гидрофобных нуклеиновых оснований [8].
Переход РНК к ДНК снижает частоту нарушений копирования, но ошибки в момент перехода возрастают. При этом, смена геномного материала сопровождается преобразованием фермента отвечающего за копирование — полимеразы. Согласно идее П. Фортера, эти реакции происходили в вирусах, а выгодой стало прохождение защитных систем клетки [25].
Эволюция РНК: увеличение количества информации генома
С появлением белкового синтеза в результате отбора, РНК-полимераза сняла с рибозимов обязанность репликации и позволила увеличить количество генетической информации. Белки стали промежуточным звеном построения липидной оболочки, а эволюция плоских структур РНК, превратила их в трёхмерные скопления покрытые мембраной [26]. Независимость от сульфида цинка была ещё невозможна, но появились пузыревидные структуры напоминающие вирусы не только механизмами репликации, но и размерами геномов.
В ходе естественного отбора, вирусы и плоские первоначальные организмы создавали новые типы нуклеиновых кислот: метил-РНК, урацил-ДНК и современную ДНК с тимином [1]. Эти кислоты использовали протоклетки позволяющие увеличивать размер и стабильность генома. Изобретение ДНК и совершенствование её копирования во множестве линий вирусов, привело к обильному разнообразию ферментов работающих с ней. Углубляясь в опыт прошлых глав, можно подытожить — надёжная репликация ДНК знаменует скорое объединение генетических элементов в большие геномы и последующий исход из источников возникновения не заставит себя ждать.
Дальнейшая эволюция: статистика и происхождение эукариот
Остался неразрешённый вопрос перехода количества в качество — о структуре клетки. Форму эукариота поддерживает цитоскелет из тонких и толстых белковых трубочек, а моторные белки перемещают компоненты клетки и обеспечивают её подвижность. Деление и слияние мембран регулируется специальными белками. Благодаря этому, большинство эукариот способны к фагоцитозу — поглощению частиц внешней среды внутрь.
Ещё одними важными органеллами являются митохондрии, которые имеют собственную генетическую систему. Их сходство с аэробными бактериями и пластидами стало первым этапом понимания происхождения эукариот. Пластиды и митохондрии образуются только в процессе деления, указывающего на происхождение от бактериальных симбионтов попавших в цитоплазму [34].
В 2015 году найдены археи близкие к эукариотам во множестве компонентов (рис. 4). Экспедиция, изучавшая геотермальные поля в Северной Атлантике, после сбора осадков населённых бактериями и археями, провела анализ их ДНК. Он показал преобладание в той локации вида архей относящегося к некультивируемой группе глубоководных архей (deep-sea Archaea group) [35]. После сбора и прочтения генома средствами вычислительной биологии, установленный вид оказался ближе к эукариотам, чем все известные ранее. Вид обладает большим набором сигнальных белков, которые в эукариотах регулируют: перестроение цитоскелета, сигналы между мембраной, цитоплазмой и ядром, деление клеток и другие функции.

В ходе эволюции эукариотам пришлось подчинить себе внутриклеточные симбиотические бактерии, вслед за тем, появился новый биохимический путь. После симбиоза с митохондриями аэробное дыхание повышает эффективность использования пищи. Десятки кластеров глубоководных организмов независимо друг от друга приручили бактерии, окисляющие сероводород или метан [1]. Благодаря этому, эукариоты приобрели функции фиксации азота, разложения целлюлозы, синтеза витаминов и пр. Но не надо захлёбываться серотониновой пеной, ведь такой вектор эволюции кажется эгоистичным. Сложно сказать, существуют ли живые организмы только для пользы репликации генома или нет. Но, в сравнении с короткой жизнью всего организма, часть информации нуклеиновых кислот существует невероятно продолжительное время передаваясь при размножении и создавая новую структуру носителя [22].
Заключение:
Нами были описаны места возможного возникновения абиогенного синтеза органических соединений с содержанием нужных для этого веществ. А также на молекулярном уровне разобраны реакции получения органических соединений из простых микроэлементов на примерах работ А. Опарина и Д. Сазерленда. Дальнейшую же эволюцию полученных биомолекул объясняют рассмотренные теории А. Маркова и П. Фортера, которые позже подтверждаются исследованиями в геотермальных полях Северной Атлантики. На протяжении всего текста можно было наблюдать уникальную биохимическую эволюцию и усложнение переносимой информации, закономерности которой описываются лишь свойствами химических веществ.
Закончу статью словами эволюционного биолога Ричарда Докинза: «Все живое эволюционирует в результате дифференциального выживания реплицирующихся единиц».
Литература:
1 — Михаил Никитин: «От туманности до клетки. Происхождение жизни»;
2 — Роберт Хейзен: «История Земли»;
3 — KhanAcademy: раздел «ДНК. Молекулярная генетика»;
4 — Опарин Александр: «Возникновение жизни на земле»;
5 — Organic compound synthesis on the primitive earth // Science — July 1959: vol. 130, no. 3370;
6 — KhanAcademy: раздел «Стереохимия»;
7 — Евгений Кунин: «Логика случая. О природе и происхождении биологической эволюции»;
8 — A semi-synthetic organism with an expanded genetic alphabet // Nature, 2014, advance online publication;
9 — Physico-chemical and evolutionary constraints for the formation and selection of first biopolymers: towards the consensus paradigm of the abiogenic origin of life // Chemistry & Biodiversity, 2007, vol. 4;
10 — α-Hydroxy and α-Amino Acids Under Possible Hadean, Volcanic Origin-of-Life Conditions // Science — October 2006: vol. 314, no. 5799;
11 — On the origin of life in the zinc world: 1. Photosynthesizing, porous edifices built of hydrothermally precipitated zinc sulfide as cradles of life on Earth // Biol. Direct, 4 (2009);
12 — An Origin-of-Life Reactor to Simulate Alkaline Hydrothermal Vents // J. Mol. Evol., 79, (2014);
13 — On the origin of life in the zinc world. 2. Validation of the hypothesis on the photosynthesizing zinc sulfide edifices as cradles of life on Earth // Biol. Direct, 4 (2009);
14 — KhanAcademy: раздел «Фотосинтез»;
15 — Origin of first cells at terrestrial, anoxic geothermal fields // Proc. Natl. Acad. Sci., 109 (2012);
16 — Lost City в Атлантическом океане;
17 — Марков Александр: «Рождение Сложности»;
18 — Элементы: «Новое в теории появления жизни»;
19 — Элементы: «Химикам удалось стабилизировать абиогенный синтез сахаров»;
20 — Synthesis of activated pyrimidine ribonucleotides in prebiotically plausible conditions // Nature — May 2009: vol. 459;
21 — Элементы: «В поисках начала эволюции»;
22 — Ричард Докинз: «Эгоистичный ген»;
23 — Валентин Пармон: «Естественный отбор среди молекул»;
24 — The origin of viruses // Research in Microbiology, 2009, vol. 160;
25 — The two ages of the RNA world, and the transition to the DNA world: a story of viruses and cells // Biochimie, 2005, vol. 87;
26 — ПостНаука: «Происхождение жизни: от РНК-мира до последнего общего предка всего живого»;
27 — KhanAcademy: раздел «Химическая связь и структура молекул»;
28 — Биомолекула: «Липидный фундамент жизни»;
29 — KhanAcademy: раздел «Химия»;
30 — Фрэнсис Эшкрофт: «Искра жизни. Электричество в теле человека»;
31 — KhanAcademy: раздел «Мембранный транспорт»;
32 — Древние системы натрий-калиевого гомеостаза клетки как предшественники мембранной биоэнергетики // Биохимия, 2015. Т. 80. Вып. 5;
33 — KhanAcademy: раздел «Строение клетки»;
34 — Complex archaea that bridge the gap between prokaryotes and eukaryotes // Nature advance online publication (2015);
35 — Asgard archaea illuminate the origin of eukaryotic cellular complexity // Nature, advance online publication (2017);
36 — KhanAcademy: раздел «Жизнь на Земле и во Вселенной».


