
Проведены 3 пилотных исследования, в которых предложены новые методы лечения этого распространённого и довольно-таки тяжёлого заболевания.
В первом исследовании, включавшем всего 12 человек и не имевшем контрольной группы, в качестве терапевтического агента был исследован известный галлюциноген грибного происхождения – псилоцибин.
Лекарство вводилось внутрь в дозе 10 мг и 25 мг с интервалом в 1 неделю. Исход терапии прослеживали вплоть до 3 месяцев с момента получения второй дозы. В течение всего периода наблюдений состояние пациентов существенно улучшилось. Несмотря на то, что к концу эксперимента у 5 из 12 человек случился рецидив, исход лечения следует признать удовлетворительным, так как участвовавшие в нём пациенты не отвечали на другие лекарства и страдали от депрессии продолжительное время.
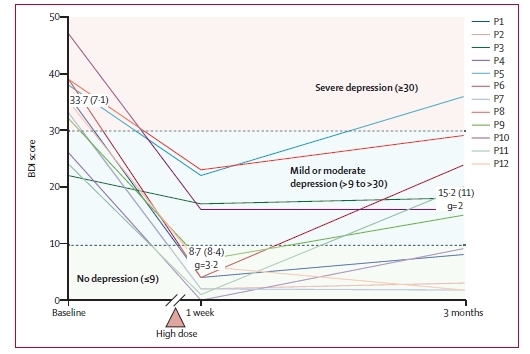
Исходы лечения депрессии псилоцибином.
Безусловно, как отмечают сами авторы исследования, рано делать серьёзные выводы о вводе в клиническую практику нового лекарственного средства, пока не будет проведено исследование с необходимыми контрольным группами. Тем не менее, не принимать во внимание полученные факты, на мой взгляд, нельзя.
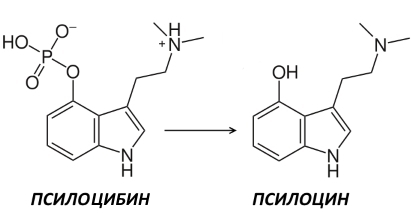
С одной стороны действие псилоцибина, превращающегося в организме человека в псилоцин, может быть объяснено в рамках классической теории о недостаточной серотонинергической передаче, которая, как полагают, имеет место при депрессии: псилоцин является агонистом 5-HT2A, 5-HT1A, 5-HT1D и 5-HT2C рецепторов.
Удивляет, однако, 3 момента, которым нельзя найти простое объяснение. Во-первых, быстрота наступления эффекта: существенное снижение симптомов по данным опросника наступило практически у всех пациентов уже через неделю после приёма последней дозы. Во-вторых, его длительность – до 3 месяцев. И в-третьих, производимый лекарством эффект. По шкале ком Глазго QIDS, которая оценивает тяжесть заболевания, достигнуто снижение баллов более чем 3 раза через неделю после терапевтического вмешательства и в 2 раза после 3 месяцев.
Однако если терапевтический потенциал псилоцибина осознавался достаточно давно, то авторы второго исследования отличились оригинальностью и использовали в качестве лечебного фактора гипертермию – нагревание всего тела до температуры выше 38 °С.
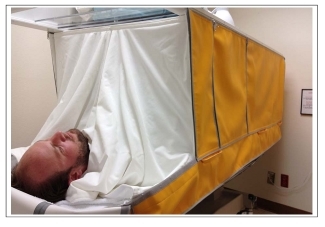
Данное исследование страдает теми же недостатками, что и предыдущее – небольшой выборкой и не совсем адекватным контролем (контрольную группу также нагревали, но до меньшей температуры). Тем не менее, несмотря на эти недостатки, показано, что в ходе лечения удалось ощутимо и надолго уменьшить тяжесть заболевания.
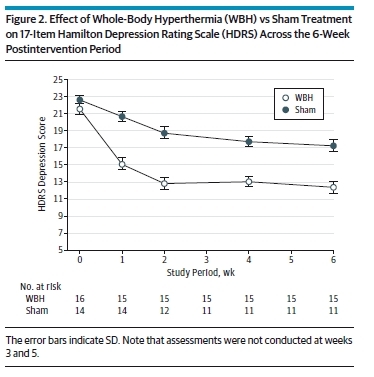
Исходы лечения депрессии гипертермией.
Механизм действия повышенной температуры на ход депрессии остаётся невыясненным. Предполагается, что нагревание способствует активации определённых частей мозга, в частности, ядер шва, относящихся к серотонинергической системе и отвечающие за регуляцию настроения.
Третье исследование, в отличие от первых двух, являлось не клиническим, а экспериментальным. Оно проводилось на мышах и касалось антидепрессантного действия ещё одного вещества с ограниченным оборотом – кетамина, который применяется в качестве анестезиологического пособия.
В отличие от традиционных антидепрессантов, являющихся веществами, так или иначе повышающими уровень норадреналина и/или серотонина в мозгу, кетамин не влияет на моноаминергическую передачу – он является блокатором NMDA-рецепторов, о которых я писал. Кстати, именно по этой причине он широко используется в нейрофизиологических экспериментах в качестве вещества, вызывающего амнезию.
Важным клиническим аспектом использования кетамина в качестве антидепрессанта является быстрота наступления его действия – в течение нескольких дней, а то и часов, в то время как традиционные препараты начинают действовать после нескольких недель приёма. Правда, действие кетамина длится недолго.
Авторы публикации в престижном журнале Nature показывают, что в многочисленных экспериментальных моделях депрессии на грызунах необходимым и достаточным агентом, присутствие которого в крови животного приводит к возникновению лечебного эффекта, является метаболит кетамина – так называемое гидроксинорпроизводное 6-гидроксиноркетамин. Это вещество, в отличие от самого кетамина, не вызывает негативного влияния на психику и не блокирует NMDA-рецепторы.
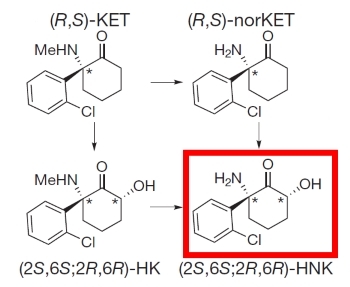
Метаболизм кетамина. 6-норгидроксикетамин обведён в красную рамку.
Предварительные выводы авторов статьи говорят о том, что действие 6-норгидроксикетамина может быть связано с влиянием на другие глутаматные рецепторы, о которых я также упоминал, — AMPA-рецепторы. Однако данное предположение требует дополнительного изучения, чем, я уверен, скоро займутся.
Как видите, на Западе к учёным, работающим в области нейробиологии, приходит понимание того, что многие запрещённые вещества имеют весьма высокий терапевтический потенциал. Остаётся пожелать регулирующим органам стран постсоветского пространства раскрыть зёнки и понять простую истину: необоснованные запреты могут привести к отставанию в развитии психиатрии и, как следствие, к невосполнимой утрате здоровья нации.
Всем не болеть!
Использованная литература:
http://archpsyc.jamanetwork.com/article.aspx?articleid=2521478
http://www.nature.com/nature/journal/vaop/ncurrent/full/nature17998.html
http://www.thelancet.com/journals/lanpsy/article/PIIS2215-0366%2816%2930065-7/abstract
http://journal.frontiersin.org/article/10.3389/fphar.2013.00161/full

