Работа по нему Alan Saghatelian и соавт. была опубликована в Nature Communications.
Исследование началось с того, что учёные обнаружили PIGBOS в митохондриях.
Первая попытка обнаружить белок PIGBOS посредством зеленого флуоресцентного белка (GFP) не удалась. Микропротеин был слишком мал по сравнению с размером GFP. Команда учёных решила эту проблему, попробовав менее распространенный подход, называемый разделенным GFP, в котором они объединили лишь небольшую часть GFP, называемую бета-версией, с PIGBOS.
Исследователи смогли увидеть PIGBOS и изучить, как он взаимодействует с другими белками. Когда они нанесли на карту местоположение PIGBOS, они поняли, что он находится на внешней мембране митохондрий, в готовности вступить в контакт с белками на других органеллах. Они были удивлены, увидев, что PIGBOS взаимодействует с белком под названием CLCC1, который является частью органеллы, называемой эндоплазматическим ретикулумом (ER).
«PIGBOS выполняет роль соединения между митохондриями и ER», — говорит ещё один соавтор работы, Qian Chu. «Раньше мы не видели этого в микропротеинах — и редко встречали в обычных белках».
Исследователи обнаружили, что PIGBOS фактически связывается с CLCC1, чтобы регулировать стресс в ER. Без PIGBOS ER, скорее всего, будет испытывать стресс, который приводит к цепочке событий, когда клетка пытается вычистить вредные деформированные белки (ответ на неправильное сворачивание белка, UPR). Если клетка не может избавиться от этих белков, она инициирует последовательность самоуничтожения и погибает.
Ученые не ожидали увидеть роль митохондриального белка в реакции UPR. Это новое понимание PIGBOS открывает двери для будущих методов лечения, которые могут быть направлены на стресс клетки.
«В будущем мы могли бы рассмотреть вопрос о том, как PIGBOS участвует в таких заболеваниях, как рак», — говорит Q. Chu. «У больных раком ER более стрессовый, чем у нормального человека, поэтому регуляция стресса ER может быть хорошей целью».
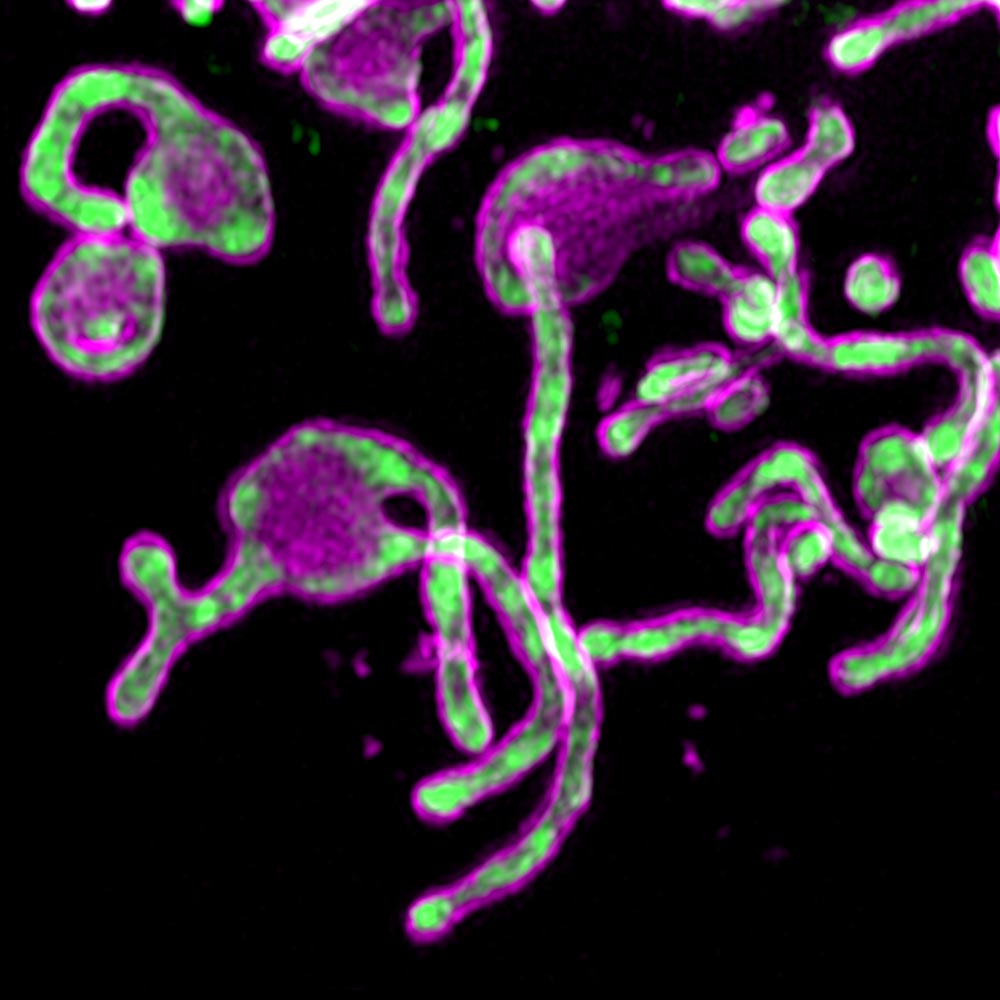
Рис. 1. Визуализация микропротеина PIGBOS
www.salk.edu/news-release/mysterious-microproteins-have-major-implications-for-human-disease
Исследователи заинтересованы в изучении роли других митохондриальных белков в стрессе ER, а также в изучении того, как PIGBOS работает в модели на животных. Команда также продвигается вперед в характеристике обширной библиотеки микропротеинов, которые могут иметь решающее значение в клеточной биологии.
Что же такое микропротеины?
Термин «микропротеины» относится к небольшим белкам, которые кодируются маленькими открытыми рамками считывания (small open reading frames, smORF). Достижения в области технологий геномики и протеомики показывают, что геномы млекопитающих предположительно содержат от сотен до тысяч микропротеинов, кодируемых smORFs. Как большая и пока ещё слабо изученная часть генома, микропротеины представляют большую возможность получить новое понимание современной биологии.
Не случайно, американский журнал The Scientist назвал микропротеины «темной материей человеческого протеома». Хотя первый из них, Id, был открыт ещё около 30 лет назад. Общей характеристикой семейства белков Id у млекопитающих является их регуляция выбора клеточной судьбы. Белки Id действуют в различных тканях и клетках, включая миобласты, нервную систему и иммунную систему. Помимо того, что они действуют как модуляторы механизма транскрипции и влияют на судьбу клеток развития, Id-белки также влияют на контроль клеточного цикла и сверх экспрессируются в различных опухолях человека. Молекулярная функция белков Id в процессах развития хорошо изучена, но мало известно известно пока о функции белков Id у взрослых.
К настоящему времени хорошо охарактеризовано лишь несколько smORF и микропротеинов. Например, некоторые специфичные для мышц smORF позволили описать новые пути, которые контролируют работу и развитие мышц. Микропротеин человека MOTS-C регулирует метаболический гомеостаз, микропротеин NoBody (non-annotated P-body dissociating polypeptide) взаимодействует с белками, расщепляющими мРНК, которые являются молекулярными компонентами первой ферментативной стадии в пути распада мРНК. А микропротеин, под названием CYREN регулирует выбор пути репарации ДНК во время клеточного цикла.
Известный на сегодня механизм действия микропротеинов заключается в подавлении образования белковых комплексов. И вот какой это имеет вид. Многие белки исполняют свои функции, действуя как часть мультибелковых комплексов. Образование этих комплексов строго регулируется и опосредуется доменами межбелкового взаимодействия. Нарушение комплекса или способности белков образовывать гомодимеры, гетеродимеры или мультимеры могут иметь серьезные последствия для клеточной функции. В связи с этим образование димеров и мультимеров может быть нарушено микропротеинами. Микропротеины ведут себя как посттрансляционные регуляторы, образуя гомотипические димеры со своими мишенями, и действуют посредством доминантно-негативного подавления функции белкового комплекса.
Проще говоря, микропротеины вмешиваются в сложную работу более крупных белков, ингибируя одни клеточные процессы и стимулируя другие. Как показывают исследования, действие микропротеинов является эволюционно консервативным и общим как для животного, так и растительного царства. Результаты первичных исследований показывают, что микропротеины участвуют в иммунных процессах, контролируют разрушение дефектных молекул РНК, защищают бактерии от жары и холода, диктуют период цветения растений, служат источником токсинов многих видов ядов животных. По мнению учёных, по всей видимости, микропротеины задействованы во всех биологических процессах. Просто раньше на них не обращали внимания.
Вероятно, что многие другие ключевые клеточные процессы также опосредованы ещё неописанными микропротеинами. И обнаружение и характеристика smORFs и микропротеинов являются важной исследовательской задачей.
Несмотря на остающиеся загадки, ученые уже тестируют потенциальное применение данных молекул. Одна компания продает инсектициды, полученные из микропротеинов, содержащихся в яде австралийского атрацида. В рамках клинических испытаний проверку проходит контрастное вещество, основанное на другом мельчайшем протеине, содержащемся в яде скорпиона. Задача этого вещества состоит в выделении границ опухолей, чтобы хирурги могли извлекать их с большей точностью. Многие фармацевтические компании сейчас ищут микробелки с медицинским потенциалом.
Насколько они могут быть крошечными, до сих пор неясно. Дрозофилам нужен микропротеин с 11-ю аминокислотами, чтобы у них выросли нормальные лапки, а некоторые микробы могут вырабатывать белки длиной менее десяти аминокислот. Но даже самые крупные микропротеины не дотягивают до протеинов среднего размера, таких как альфа-амилаза, 496-аминокислотного фермента, содержащегося в нашей слюне и расщепляющего крахмал.
Лишь недавнее выявление небольшого количества микропротеинов связано с установленным около 20 лет назад критерием распознавания генов. Когда ученые анализируют геном организма, они часто сканируют открытые рамки считывания (ОРС). Чтобы не потонуть в огромном объеме данных, в прошлом исследователи, как правило, исключали любую ОРС с протеином меньше, чем 100 аминокислот в эукариотах или 50 аминокислот в бактериях. Например, в дрожжах это условие ограничило список ОРС примерно до шести тысяч.
Ослабление этого критерия показывает, что клетки содержат значительно больше ОРС. Ранее в этом году учёные выявляли фрагменты генома микробов, населяющих четыре части человеческого тела, включая кишечник и кожу. При поиске небольших ОРС, способных кодировать белки длиной от пяти до 50 аминокислот, исследователи выявили около четырех тысяч семейств потенциальных микропротеинов. Почти половина из них не похожа на известные белки, но последовательность одной небольшой ОРС позволяет предположить, что соответствующий белок находится в рибосомах — а это указывает на то, что он может играть какую-то основополагающую роль. Когда ученые упускали из виду маленькие ОРС, пропускались не просто гены с какими-то редкими функциями, а гены с ключевыми функциями.
Другие клетки также содержат огромное количество коротких ОРС: дрожжи, к примеру, способны произвести более 260 тысяч молекул, обладающих спектром от двух до 99 аминокислот. Но клетки почти наверняка не используют все эти ОРС, и некоторые из производимых ими аминокислотных цепочек могут быть нефункциональными.
Weissman и соавт. обнаружили микропротеины другим способом: применив изобретенный ими метод, направленный на более масштабное выявление того, какого рода протеины производят клетки. Чтобы сформировать любой белок, клетка сначала копирует ген в РНК-мессенджер. Затем рибосомы считывают мРНК и связывают аминокислоты в определенном порядке. Путем секвенирования мРНК, прикрепленных к рибосомам, Вайссман и его команда точно определяют, какие из них фактически превращаются в белки, и где на РНК рибосома начинает «читать». В исследовании клеток 2011 года ученый со своей командой применил данный метод профилирования рибосомы, называемый также Ribo-seq, к эмбриональным стволовым клеткам мыши и обнаружил, что клетки производят тысячи непредвиденных белков, в том числе многие, в которых количество аминокислот будет ниже порога в 100 единиц. «Было совершенно ясно, что в рамках стандартного подхода игнорировалась обширная вселенная протеинов, многие из которых были короткими», — говорит Вайссман.
Saghatelian с коллегами применили третий подход для обнаружения изобилия микропротеинов в наших собственных клетках. Ученые использовали масс-спектрометрический анализ, в рамках которого протеины расщепляются на фрагменты, сортируемые в соответствии с массой, с целью выявления опознавательного спектра каждого протеина. Сагателян с коллегами применили этот метод к смесям протеинов из клеток человека, а потом вычли из них признаки известных видов протеинов. Этим методом были выявлены спектры 86 прежде не известных крошечных белков, самые маленькие из которых были длиной в 18 аминокислот, как отмечали ученые в статье журнале Nature Chemical Biology в 2013 году.
Маленький размер ограничивает потенциал протеина. Более крупные протеины соединяются в сложные формы, направленные на осуществление определенных функций, например, катализации химических реакций. Протеины, содержащие от 50 до 60 аминокислот, вероятно, не будут образовывать соединений. И поэтому, они не подходят для образования энзимов или структурных протеинов.
Однако их малые размеры также открывают определенные возможности. Они достаточно крошечные, чтобы встраиваться в укромные уголки больших белков, которые функционируют как каналы и рецепторы. Маленькие белки часто делят короткие отрезки аминокислот со своими более крупными партнерами и поэтому могут связываться и изменять активность этих белков. Связанные микропротеины могут также направлять большие молекулы в новые места — например, способствуя их проникновению в клеточные мембраны.
Из-за своего притяжения к более крупным протеинам малые протеины могут дать клеткам обратимый способ активирования или дезактивации более крупных протеинов. В исследовании 2016 года, опубликованном в журнале PLOS Genetics, Stephan Wenkel с коллегами генетически модифицировали растения Arabidopsis, чтобы произвести дополнительное количество двух малых протеинов. Растения обычно расцветают в тот период, когда день достаточно продолжителен, но после произведения на свет избыточного количества двух видов микропротеинов цветение задержалось. Малые протеины спровоцировали эту отсрочку, заблокировав запускающий цветение крупный протеин под названием CONSTANS. Они связывают CONSTANS с другими ингибиторными протеинами, которые его отключают.
В 2016 году Сагателян и его коллеги выяснили, что клетки человека производят протеин, содержащий 68 аминокислот, который они назвали NoBody. Этот протеин может помочь при уничтожении дефективных или ненужных молекул РНК. Название «НиКто» отражает роль этого протеина в предотвращении образования процессивных телец, загадочных кластеров в цитоплазме, где может произойти разрушение РНК. Когда не хватает протеина, образуется большее количество процессивных телец, что ускоряет разрушение РНК и изменяет внутреннюю структуру клетки. «Это доказывает, что малые протеины могут оказывать огромное воздействие внутри клетки», — отмечают учёные.
Мышцы зависят от множества разных микропротеинов. В ходе развития эмбриона отдельные мышечные клетки сливаются в волокна, которые запускают сокращение. 84-аминокислотный белок Myomixer объединяется с более крупным белком, чтобы соединить клетки, как показал Olson и соавт в 2017 году в своей работе в журнале Science. Без него зародыши мышей не могут сформировать мышцы и почти прозрачны.
Далее по мере развития в силу вступает миорегулин, способствующий регулированию мышечной деятельности. Когда мышца получает стимул, клеточное хранилище выделяет кальций, стимулируя сокращение тканей и выработку энергии. Далее ионный насос, белок под названием SERCA начинает возвращать кальций в хранилище, позволяя мышечным тканям расслабляться. Миорегулин соединяется с SERCA и ингибирует его. Этот эффект ограничивает частоту сокращения мышц, вероятно, обеспечивая запас энергии на крайний случай, например, при бегстве от хищника. Другой малый протеин, DWORF, оказывает обратное воздействие, активируя SERCA и стимулируя систематическое сокращение мышц.
Даже досконально изученные организмы, такие как бактерии кишечной палочки (Escherichia coli) таят неожиданные малые протеины, играющие важную роль. Storz и соавт. сообщили в 2012 году, что неизвестный до этого 49-аминокислотный белок под названием AcrZ помогает этому микробу выживать при воздействии некоторых видов антибиотиков, стимулируя насос, не допускающий проникновения лекарства.
яд, производимый разнообразными организмами — в том числе пауками, сколопендрами и ядовитыми моллюсками — также изобилует крошечными протеинами. Многие составляющие яда обездвиживают или убивают, блокируя каналы для натрия или других ионов, необходимых для передачи нервных импульсов. Малые протеины «наносят удар по этим ионным каналам с удивительной точностью и мощью, говорят учёные. Они являются главными составляющими ядов, и именно с ними связана большая часть фармакологических и биологических последствий.
Гигантское питающееся рыбой австралийское насекомое, например, не просто полагается на острые челюсти и пикоподобные ротовые части, чтобы одолеть свою добычу. Оно вводит своим жертвам дозу, содержащую более 130 протеинов, в составе 15 из которых менее 100 аминокислот.
В отличие от крупных протеинов, таких как антитела, микропротеины, поступающие в организм из таблеток или инъекций, могут проникать в клетки и модифицировать их функции. Каптоприл, первое из класса лекарств от высокого давления, известное как ингибитор ангиотензинпревращающего энзима, был разработан из малого протеина, содержащегося в яде обыкновенной жарараки, вида ядовитых ямкоголовых змей. Это лекарство, одобренное для продажи в Соединенных Штатах в 1981 году, было обнаружено случайно, еще до того, как ученые признали малые протеины как отдельную группу. Пока что лишь несколько микропротеинов попали на рынок или на клинические испытания.
Ученые, занимающиеся исследованием рака, пытаются применить микропротеин, содержащийся в яде желтого скорпиона, распространенного в Африке и на Ближнем Востоке. Эту молекулу таинственным образом тянет к опухолям. Добавляя ее к флуоресцентному окрашивающему веществу, ученые рассчитывают подсветить границы опухолей мозга, чтобы хирурги могли безопасно вырезать пораженные раком области..Она подсвечивает опухоль. Таким образом можно увидеть ее границы и выявить наличие метастаз. В ходе клинических испытаний сейчас исследователи оценивают, поможет ли двойственная молекула хирургам удалять опухоли мозга у детей.
Насколько важную роль малые протеины сыграют в медицине, до сих пор неизвестно, однако они уже перевернули ряд утверждений биологов. Norbert Hübner из Центра молекулярной медицины Макса Дельбрюка в Берлине вместе с коллегами обнаружили десятки новых микропротеинов в клетках человеческого сердца. Группа выявила неожиданный их источник: короткие последовательности внутри длинных некодирующих РНК, то есть в разновидности, которая, как ранее считалось, не производит протеинов. Идентифицировав 169 длинных некодирующих РНК, вероятно читаемых рибосомами, Хюбнер со своей командой использовал один из видов массовой спектрометрии, чтобы подтвердить, что более половины из них производят микропротеины в клетках сердца. их статья с результатами работы вышла в этом году в журнале Cell.
Последовательности ДНК других крошечных протеинов также можно встретить в нетрадиционных местах. Например, некоторые находятся у открытых рамок считывания, ОРС, более крупных протеинов. Ученые ранее полагали, что эти последовательности помогают контролировать выработку более крупных протеинов, но редко сами производят протеины. Некоторые кодирующие последовательности недавно выявленных микропротеинов кроются даже в последовательностях, кодирующих другие, более длинные протеины.
Эти геномные сюрпризы могут пролить свет на то, как возникают новые гены, говорит биолог-специалист по эволюционным системам Anne-Ruxandra Carvunis из Питтсбургского университета в Пенсильвании. Ученые ранее считали, что большинство генов появляется, когда существующие гены размножаются или сливаются, или когда виды обмениваются ДНК. Однако, по мнению Карвунис, микропротеины указывают, что протогены могут формироваться, когда мутации задают новый старт и останавливают сигналы в некодирующей части генома. Если получающаяся в результате ОРС производит полезный протеин, новые последовательности останутся в геноме и пройдут через процесс естественного отбора, в дальнейшем эволюционируя в более крупные гены, кодирующие более сложные протеины.
В исследовании 2012 года Карвунис вместе с коллегами обнаружила, что дрожжи трансформируют более тысячи коротких ОРС в протеины. А это говорит о том, что эти последовательности являются протогенами. В новом исследовании Карвунис со своей командой провела испытания, могут ли молодые ОРС быть полезны для клеток. Они генетически изменили дрожжи, чтобы увеличить результат из 285 недавно эволюционировавших ОРС, большинство которых ориентированы на молекулы меньшего размера, чем стандартно содержат протеины или немногим больше этого количества. У почти 10% протеинов повышение их уровней усиливало клеточный рост, по меньшей мере, в одной среде.
«Микропротеины представляют собой быстро развивающуюся область», — говорит A. Saghatelian. «Но я думаю, что это наше исследование действительно повлияло на текущее понимание влияния микропротеинов на биохимию и клеточную биологию».
Ссылки:
Regulation of protein function by ‘microProteins’
www.ncbi.nlm.nih.gov/pmc/articles/PMC3024132
New universe of miniproteins is upending cell biology and genetics
www.sciencemag.org/news/2019/10/new-universe-miniproteins-upending-cell-biology-and-genetics
Regulation of the ER stress response by a mitochondrial microprotein
www.nature.com/articles/s41467-019-12816-z
