
Выполнять роль рядовых бойцов на передней линии фронта в борьбе с внешними угрозами приходится бактериям, время от времени атакуемым вирусами-бактериофагами. Для победы над врагом бактерии в процессе эволюции тоже выработали свои иммунные механизмы — доспехи, способные защитить их от смертоносных инфекций. Один из таких механизмов — CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats), система, позволяющая бактерии сохранять в своей «базе данных» фрагменты генома бактериофагов, с которыми ей уже приходилось встречаться в прошлом, с тем, чтобы быстрее обнаружить и остановить вторжение в будущем. С 2012 года система CRISPR также была рекомендована учеными, как революционная технология редактирования генома.
В мире, где бесчисленные крошечные микробы способны заразить и убить, такая защита становится нашим самым эффективным средством сопротивления. Системой CRISPR, как считается, располагает примерно половина известных научному сообществу бактерий. Изучением ее защитных механизмов занимается команда специалистов из лаборатории профессора молекулярной биологии и микробиологии Эндрю Камилли (Andrew Camilli).
«Я постоянно поражаюсь, как бактерии способны пережить подобный натиск», — говорит Эндрю Камилли. «… Фаги очень коварны». Профессор связывает способность выживания некоторых бактерий с типом иммунной системы «CRISPR/Cas». Но, как выяснилось в ходе проведенных исследований, такого рода системой адаптируемого иммунного ответа располагают не только клетки бактерий. В ходе исследований ученые пришли к выводу: бактериофаги сумели отыскать противоядие на этом уровне защиты и создать «противоиммунную» систему, чего, с учетом внешней простоты организации и строения этих микроорганизмов вряд ли кто-то мог ожидать. И, тем не менее, эти простые на первый взгляд структуры в составе небольшого комплекта генов, заключенных в белковую оболочку, способны мимикрировать с невероятной быстротой, проявляя чудеса изменчивости.
Создание такой противоиммунной системы, по мнению ученых, стало результатом случайной рекомбинации генов бактериофага и бактерии на каком-то витке эволюции. Подобное в микромире отнюдь не редкость: мириады бактерий то и дело заражаются мириадами вирусов, и иногда случайные фрагменты бактериальной ДНК оказываются встроены в геном фага, так и оставаясь в нем дополнительным грузом. Так в теории могло произойти и с фагом ICP1, который, как обнаружил Камилли с коллегами, сумел «позаимствовать» весь комплект рабочих генов системы CRISPR бактерии.
Вирус был выявлен учеными при анализе проб, полученных в районах эпидемий холеры за период в 10 лет. Авторы провели скрининг бактериофагов, способных поражать холерные вибрионы, и обнаружили, что в разных случаях набор этих вирусов может кардинально отличаться. И только лишь единственный ICP1 обнаружился во всех пробах. Пытаясь найти объяснение этой феноменальной стойкости
бактериофага, ученые секвенировали его геном и обнаружили полный набор генов системы CRISPR. Таким образом, располагая в своей «библиотеке» генами ДНК самой бактерии, ICP1 вносят в работу ее защитных систем полный хаос, лишая возможности эффективно противостоять инфекции.
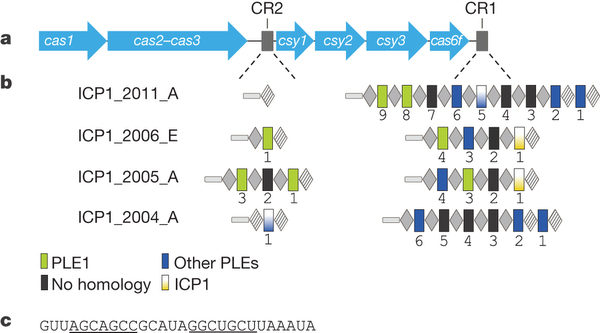
Камилли признает, что «… Обнаруженный фаг, называемый ICP1, способен «украсть» весь набор рабочих CRISPR/Cas генов адаптивной иммунной системы бактерии, и нет ни одного примера любого другого возбудителя — будь то паразит, бактерия или вирус, которые смогли бы повторить нечто подобное. Это самое удивительное открытие из всех, которые нам удалось сделать».

Вирусы — не более, чем белковые оболочки, обернутые вокруг ДНК, и, все же, их возможности продолжают удивлять нас, заставляя думать, что они не так просты, как представляются на первый взгляд.
Простейшие вирусы, как утверждают некоторые исследователи, даже не живы. На базовом уровне, это просто белковые оболочки, обернутые вокруг ДНК. И, тем не менее, они способны развиваться и меняться, а с учетом результатов исследований это может означать, что они гораздо более приспособлены к борьбе с иммунитетом человека, чем думали ученые.
Рабочая система CRISPR/Cas, найденная в бактериофаге, может помочь вирусной атаке и сломать защитный барьер бактерии. Если это действительно так, то исследования команды Камилли может иметь огромное значение для медицины. Как только ученые поймут, как именно фаг использует CRISPR/Cas, заражая и убивая бактерии, можно будет использовать полученные знания, чтобы синтезировать фаги, которые смогут противодействовать заболеваниям, таким как холера значительно более эффективно, чем существующие антибиотики.
Резистентные бактерии, стойкие к большинству современных антибиотиков уже обнаруживаются по всему миру. С ограниченными возможностями современных лекарственных препаратов, лечение все чаще оказывается неэффективным. Бактериофаги способны предложить альтернативную схему лечения. В сравнении с разработкой новых антибиотиков занимающих годы и стоящих многие миллионы долларов, синтез нового фага оказывается несоизмеримо более прост. «Вы можете выделить фаги, которые окажутся способны убить конкретный вид бактерий всего за одну неделю», — резюмирует профессор Камилли. Отчет о результатах работы группы Камилли был опубликован сразу в нескольких авторитетных изданиях, включая Nature (23.02.2013 года).
Последние исследования в этом направлении
Исследования профессора Камилли, ставшие достоянием научного сообщества в 2013 году совсем недавно нашли еще одно подтверждение. На этот раз способность фагов красть участки цепочки ДНК, принадлежащих поражаемым ими бактериям подтвердила группа ученых-микробиологов из университета Британской Колумбии (University of British Columbia), Канада под руководством известного вирусолога Кертиса Саттла (Curtis Suttle).
Они обнаружили, что вирус типа Cyanophage N1, который проявляет агрессию в отношении некоторых видов бактерий, обитающих в пресноводных водоемах, активно использует «украденные» на этапе своего эволюционирования участки ДНК этих «бактерий» для того, чтобы подавить реакцию их иммунной системы. И вновь подтвердилось, что этот тип вируса располагает в своем коде фрагментами CRISPR- последовательностей ДНК, используемыми самими бактериями для защиты от вирусных нападений.
«Мы смогли наблюдать, как вирус атакует иммунную систему бактерий, используя их участки генетического кода CRISPR» — рассказывает Саттл, — «Такое поведение цианофага будет уместно сравнить с действиями хакера, атакующего компьютерную систему и немедленно исправляющего последствия своих действий для того, чтобы быть уверенным, что другие хакеры уже не используют обнаруженную им лозейку».
«Бактерии и вирусы имеют общую эволюционную историю, уходящую назад на миллиарды лет» — продолжает Саттл, — «И в какой-то момент этой истории, вирус N1 позаимствовал несколько защитных CRISPR-последовательностей у цианобактерий вида Nostoc, Anabaena и их ближайших соплеменников. А теперь он использует украденные вещи для того, чтобы успешно атаковать эти бактерии».
Здесь стоит добавить, что бактерии Nostoc и Anabaena, поражающиеся цианофагом N1, относятся к виду цианобактерий, обитающих на земном шаре почти повсеместно. Их предки некогда выработали большую часть кислорода, находящегося в атмосфере Земли, а бактерии Nostoc и их ближайшие «родственники» остаются источником весьма и весьма значительной части жизненно важного для нас кислорода и сегодня.
Подробнее с результатами исследований группы Саттла вы можете познакомиться на страницах журнала mBio Американского общества микробиологии 14.06.2016 года.
На этом всё, с вами был Dronk.Ru. Не забывайте возвращать деньги за покупки в Китае и подписываться на наш блог, будет ещё много интересного.

Рекомендуем:
— Экономим до 8% с каждой покупки на AliExpress и других интернет-магазинах Китая
— Почему интернет-магазины отдают деньги за покупки?
— Верните свои деньги — Выбираем кэшбэк-сервис для Aliexpress
— История развития Dronk.ru — от выбора квадрокоптеров до возвращения денег за покупки на AliExpress и не только
— Лучший кэшбэк сервис или 5 основных критериев оценки кэшбэк-сервиса


